-
科室:
小儿血液科
-
别名:
儿童急性非淋巴细胞性白血病
小儿急非淋
小儿急性非淋白血病
-
症状:
暂无
-
发病部位:
暂无
-
多发人群:
婴幼儿
-
相关疾病:
暂无
白血病是一种干细胞或克罗恩病,即由一个干细胞发生恶性变引起的疾病,白血病细胞来源于一个突变的异常干细胞,白血病细胞增殖失控,分化成熟能力丧失。由于其增殖与分化过程失衡,致使白血病细胞在骨髓中大量聚积,骨髓压力增加,窦样隙屏障可能被破裂,使各阶段不成熟的细胞进入血液。白血病细胞离开血管进入组织也不像正常成熟细胞那样在短期内死亡,而是保持着继续分裂的能力,形成脏器内白血病细胞浸润,引起器官及组织受累的各种相应症状和体征。 白血病的分类根据细胞的分化程度、自然病程的长短,分为急性和慢性两大类,再根据细胞的类型分为若干型。如急性白血病又分为急性淋巴细胞白血病和急性非淋巴细胞白血病。随着生物分子学的进展,对儿童AML的发病机制及生物学特性有了更进一步的了解,目前在合理治疗后约有30%~45%的患儿可获得长期无病生存,较急性淋巴细胞白血病(ALL)的预后仍然明显差。 急性髓细胞性白血病(acute myeloid leukemia,AML)在分子生物学改变及化疗反应方面,儿童AML与成人(<50岁)相似。婴幼儿的AML比成人易发生髓外白血病。在过去20年AML的治愈率约40%,远不及儿童ALL。AML第1次缓解后同胞间异基因BMT结果稍好于化疗。 儿童AML可发生于任何年龄,各年龄组发病率基本一致,在青少年略高些。不像ALL在3~4岁为高峰。男女之间无差异。AML发病与某些遗传性疾病有关,如在21-三体、范可尼贫血等病中,AML发病率较高。一些恶性肿瘤治疗后发生继发性AML可能性约5%。AML发生与某些药物治疗(如环磷酰胺、鬼臼类药物)及放射治疗有关。[收起]
白血病是一种干细胞或克罗恩病,即由一个干细胞发生恶性变引起的疾病,白血病细胞来源于一个突变的异常干细胞,白血病细胞增殖失控,分化成熟能力丧失。由于其增殖与分化过程失衡,致使白血病细胞在骨髓中大量聚积,骨髓压力增加,窦样隙屏障可能被破裂,使各阶段不成熟的细胞进入血液。白血病细胞离开血管进入组织也不像正常成熟细胞那样在短期内死亡,而是保持着继续分裂的能力,形成脏器内白血病细胞浸润,引起器官及组织受累的各种相应症状和体征。 白血病的分类根据细胞的分化程度、自然病程的长短,分为急性和慢性两大类,再根据细胞的类型分为若干型。如急性白血病又分为急性淋巴细胞白血病和急性非淋巴细胞白血病。随着生物分...[详细]
1.病因 儿童白血病的病因尚不明了,可能的发病因素包括以下几方面。 (1)理化因素:迄今为止,虽有大量有关环境因素与白血病发病相关性的研究,但确定的相关因素只有电离辐射。如苯和电离辐射的暴露与AML发病有关,但能明确的个体致病因素仅占发病数中的极少部分。对日本广岛、长崎原子弹爆炸地区生存者的研究发现,原子弹爆炸5~15年后白血病的发病率增加,AML的发病率增高20倍,其高峰在接受辐射后6~8年。白血病的发生危险性与接受的放射剂量有关。而对三里岛和切尔诺贝利核事故的随访研究尚未发现与儿童白血病发病的相关性。孕期吸烟也增高AML的发病率。在第二肿瘤中,AML是一种较常见的类型,主要与先前烷化剂如环磷酰胺、氮芥、白消安等暴露有关,常发生于第一肿瘤4~5年后,可先表现为骨髓增生异常综合征(MDS)再发展为AML,但在10~12年后AML的发病机会减少。除此以外,鬼臼毒素类药物VP-16的暴露与第二肿瘤性AML的发病有关,其发病时间常较烷化剂诱发者早。20世纪50年代有报道认为在孕妇子宫接受X线照射会增加儿童患白血病的危险,但现在对此观点尚存争议。目前也有研究认为双亲在怀孕前低水平的射线接触会增加婴儿白血病的危险。多中心的研究表明母亲孕前、孕中及父亲职业接触杀虫剂、除莠剂、杀真菌剂等与儿童白血病的发病有关。 电磁场与白血病发病的相关性早在20世纪70年代已有报告。而此后的大系列研究未证实低强度电磁场与儿童白血病及其他儿童肿瘤发病有关的假设。近年来自美国、加拿大及英国的研究结果认为暴露于高强度磁场(>0.4μT)下可能增加急性白血病的患病危险,而低强度磁场对机体的影响甚微。 最近的研究还表明家用有机溶剂与儿童急性白血病的发生有关。 职业接触苯与成人急性白血病的发生密切相关。尽管儿童ALL不可能由职业接触所致,但环境中的苯浓度日益增加可能是儿童ALL的病因之一。有研究报道居住于交通要道或加油站附近(100m以内)的儿童,发生白血病的危险性增加,此结果基于生态学研究,确切的相关性有待进一步研究证实。我国对1000余名白血病患儿研究结果显示。有46%的家庭在患儿确诊前6个月内进行过室内装修。苯导致儿童白血病的可能机制与儿童的个体易感性强、儿童毒物代谢酶,如细胞色素p4502E1、髓过氧化物酶(MPO)、谷胱甘肽硫转移酶(GSTs)等的基因多态性以及儿童体内存在固有的基因缺陷等有关。 (2)病毒:尚未证实与AML发病有关的病毒。 (3)遗传因素:至今在大多数儿童AML中未能证实遗传因素的参与,偶有同胞发病或家族性发病的报告。唐氏综合征患儿发生AML的机会比正常人群高14倍。在同卵双胎中,若一胎在6岁前发病,则另一胎发病的机会约为20%;在1岁以前发病者,另一胎发病的机会大大增加;而一胎在6岁以后发病者,另一胎的发病机会则较6岁前发病者明显下降。一些先天性骨髓性疾病中发生AML的机会也增加。现已证明某些遗传性综合征,如21-三体综合征(Down syndrome)及Fanconi贫血与白血病的易感性密切相关。英国及美国的研究表明2.3%~2.6%的儿童急性白血病与遗传因素有关。 对所有类型白血病患者的同胞、双亲及后代的调查未发现有肿瘤高发的现象。虽有同胞相继发生白血病的报告,但发生率极低。同卵双胞胎发生白血病的概率比异卵双生者大。祖父、双亲、同胞当中有遗传性缺陷者与多种类型ALL的发病有关,其中包括肌肉骨骼疾病、胃肠疾病、变态反应性疾病、遗传性心脏病及肺部疾病等。 由于近年已有足够多的长生存病例,有学者对长生存患者的后代进行了白血病相关危险性的调查,结果未发现该人群发生白血病的危险性增加。同时对健康生存的儿童白血病患儿进行了染色体稳定性的检查,无论在对照组还是博来霉素诱导畸变组均未发现染色体不稳定性的增加。与健康人群对照研究发现长生存ALL患儿的后代中先天性畸形者并无增加。 遗传与环境因素在儿童ALL的发生中具有相互作用。组织相容性白细胞抗原(HLA)被认为是白血病易感的遗传性危险因素之一。其相关性表现为在男性中最普通的等位基因HLA-DR53、HLA-DRB1?04表达增强。并且在ALL患者中发现HLA-DRB1?04的纯合基因、编码HLA-DR53特异性明显增强。HLA-DRB1?04的纯合基因与ALL的相关性在男性患者表现尤为突出。HLA-DR53与H-2Ek之间的交叉反应通过一些致癌病毒广泛地模仿HLA-DR53免疫优势抗原决定簇,而且在临近HLA-DRB4基因上额外数量的DNA证明HLA-DRB1?04可能是儿童ALL的遗传因素之一。在60例儿童ALL和78例新生儿DQA1和DQB1的等位基因对照研究中发现男性患者DQA1?0101/?0104和DQB1?0501比正常对照发生率高。这个结果提示在ALL患者中有男性相关的易感HLA系。 有人研究了谷胱甘肽S转移酶和细胞色素P-450基因在儿童肿瘤中的作用。这两种酶均参与致癌物代谢并构成成人多种癌症的高危因素,并通过NAT1和NAT2编码的N-乙酰转移酶参与香烟、环境及食物中的芳香胺的生物转化。这些快速和缓慢的乙酰化作用等位基因在多种成人实体肿瘤中起修饰作用。低叶酸盐摄取或作为亚甲基四氢叶酸还原酶(methylene tetrahydrofolate reductase,MTHFR)多态性结果的叶酸盐代谢的改变均与神经管缺陷及一些癌症有关。MTHFR多态性的改变导致胸腺嘧啶核苷池增加和高质量DNA合成,为白血病的发生提供保护,尤其与发生染色体易位的白血病密切相关。 Wiemels等报告了MTHFR多态性与MLL基因重排的婴儿白血病及TEL-AML1阳性或超二倍体儿童白血病的相关性。这些研究结果为儿童白血病不同分子生物学亚型可能有不同的病因提供了证据,同时也提示叶酸盐在儿童白血病发生中所起的作用。Krajinovic等发现GSTML裸基因型和CYP1A1基因型可有意义地预测ALL的发病危险。当NAT2缓慢乙酰化时,通常被认为与其他高危基因型如GSTML裸基因型、CYP1A?2A基因型共同作用,增加发生白血病的危险。Davies等研究发现GSTML裸基因型是对儿童AML(特别是FAB分型中的M3和M4)有预测意义的基因型。这些研究结果提示了基因与环境因素的相互作用在儿童白血病发病中的可能作用。 婴儿白血病近80%伴有发生于11q23染色体上的遗传学异常,形成MLL融合基因。11q23也常见于应用拓扑异构酶Ⅱ抑制剂所致的继发性白血病(AML)。因此Ross等学者推测婴儿白血病可能与暴露于自然状态下的拓扑异构酶抑制剂(包括咖啡因、变种的水果和蔬菜)有关,并进行了多中心的研究,结果未发现拓扑异构酶Ⅱ抑制剂类食物与各种类型ALL发病的相关性。但拓扑异构酶Ⅱ抑制剂类食物补充量增加与AML的发病具有明显的相关性。最近的体内研究证明,食物中天然存在的生物类黄酮与食品添加成分一样可引起在MLL基因断裂点区域的位点特异的DNA切割。这些结果提示母亲摄入生物类黄酮可诱发MLL基因断裂并可能在子宫内导致染色体易位,从而导致婴儿白血病的发生。吸烟、饮酒、服用某种特定的中药和导致DNA损伤的药物,接触杀虫剂可增加与MLL基因改变相关的急性白血病的发病危险。 2.既往病史 2117例ALL和650例AML的调查中发现,Down综合征、先天性心脏病、胃肠道畸形在ALL患儿中多见;Down综[收起]
1.病因 儿童白血病的病因尚不明了,可能的发病因素包括以下几方面。 (1)理化因素:迄今为止,虽有大量有关环境因素与白血病发病相关性的研究,但确定的相关因素只有电离辐射。如苯和电离辐射的暴露与AML发病有关,但能明确的个体致病因素仅占发病数中的极少部分。对日本广岛、长崎原子弹爆炸地区生存者的研究发现,原子弹爆炸5~15年后白血病的发病率增加,AML的发病率增高20倍,其高峰在接受辐射后6~8年。白血病的发生危险性与接受的放射剂量有关。而对三里岛和切尔诺贝利核事故的随访研究尚未发现与儿童白血病发病的相关性。孕期吸烟也增高AML的发病率。在第二肿瘤中,AML是一种较常见的类型,主要与先...[详细]
1.细胞癌基因与病毒癌基因 病毒、电离辐射、化学物质等如何导致白血病,机制并未完全清楚。细胞的增殖、分化和衰老死亡都是由基因决定的,显然细胞的恶性转化也必然与基因的某种改变相关联。现知动物和人类细胞以及某些种类的病毒株中都存在能诱导正常细胞恶性转化,并使其获得新生物特性的肿瘤基因,前者称为细胞癌基因(cell oncogene)或原癌基因,后者称为病毒癌基因(virus oncogene)。细胞癌基因原是正常基因的成员,他们在细胞增殖、分化、衰老死亡进程的一定时期起作用,并受内在机制的调节和节制,当这些基因异常激活转为肿瘤基因时,就具有了致癌活性。研究表明病毒癌基因并非是病毒本身固有的,而是在反复感染宿主过程中由宿主细胞的DNA片段通过重组插入到病毒基因组中的。 2.癌基因的激活 细胞癌基因异常激活转化为癌基因,是通过基因DNA结构的改变和调控失调获得的。这些包括: (1)点突变:基因DNA链上一个至数个核苷酸序列发生改变是为点突变,例如癌基因ras就是由细胞癌基因ras突变而来; (2)染色体重排:由于染色体易位、倒位、缺失等改变导致基因或其调控区DNA结构和序列改变是癌基因激活的常见方式。典型的例子是Ph染色体的形成,它是t(9;22)(q34;q11)易位形成,即9号染色体上细胞癌基因c-ABL易位到22号染色体上断裂处并形成BCR/ABL融合基因而激活; (3)基因扩增:这些基因可复制成多套拷贝,其中部分拷贝脱离染色体形成双微粒体,部分可再次整合进染色体,因此蛋白产物增加,并可能使细胞恶性转化。 3.关于抑癌基因 近年研究发现人体细胞内存在着能够抑制肿瘤形成的基因,称为抑癌基因(tumor suppressor gene),迄今报告的人类抑癌基因有RB,P53,P16,WTI等近十种。由于基因的突变、缺失可致抑癌基因的异常失活,结果往往使细胞癌基因过度表达而发生细胞转化。我们曾用PCR-SSCP(single stranded conformational polymorphism)分析和DNA印迹杂交法检测了31例儿童急性淋巴细胞白血病患儿的P16抑癌基因缺失及点突变情况,结果发现P16基因缺失率(包括点突变)为25.8%,其中纯合子缺失:B-ALL为16%,T-ALL为33%,点突变则两型中各1例。说明由于基因缺失及点突变导致P16基因灭活,在急性淋巴细胞白血病中有较高的发生率,提示与疾病的发生、发展以及预后都有密切关系。 4.病毒癌基因的致癌机理 诱发动物和成人T细胞白血病的病毒几乎都是C型反转录病毒,感染宿主细胞后,以病毒的RNA为模板在反转录酶和DNA多聚酶作用下合成了双链前病毒DNA,并进一步整合进宿主细胞的DNA中。病毒癌基因整合进宿主细胞后可以被激活表达而诱导细胞恶性转化,也可以受宿主细胞的遗传调控处于静止期,当在射线或化学物质等作用下激活时可诱发肿瘤。新近提出的病毒基因产物的反式调节作用从另一方面解释了HTLV-1型病毒的致癌作用。即这类病毒某些基因能编码一种特殊的蛋白因子,该因子不仅能增加病毒的复制而且可选择性启动宿主细胞的一定基因,例如诱导白介素2(IL-2)及其受体合成增加,进而促使T细胞恶变。 5.关于细胞凋亡 凋亡(apoptosis)是一种基因指导下的细胞主动性自我消亡过程,它是正常胚胎发生过程和成人组织器官发育中细胞清除的正常途径,当凋亡通路受到抑制或阻断就可使细胞永生化而恶变。凋亡涉及到一系列的基因调控,促进凋亡的基因有Fas,Bax,ICE,P53等,抑制凋亡的基因包括Bcl-2,Bcl-XL等。凋亡理论的提出不仅为白血病病因学和发病机制研究开辟了新领域,而且为白血病的治疗和耐药性研究提供了新思路。现知许多治疗白血病的药物如阿霉素、顺铂、依托泊苷、放线菌素D、氨甲蝶呤、阿糖胞苷等都能诱导白血病细胞发生凋亡。我科曾经研究过高三尖杉酯硷诱导HL-60白血病细胞的凋亡作用,发现该药主要是通过激活Fas蛋白,下调Bel-2蛋白,从而启动凋亡程序的。许多耐药性研究指出,白血病细胞对诱导凋亡药物的敏感性与细胞内Bcl-2基因的表达水平有关,Bcl-2表达水平越高则敏感性越差,因此检测白血病细胞Bcl-2表达水平可衡量化疗敏感性和估测预后。[收起]
1.细胞癌基因与病毒癌基因 病毒、电离辐射、化学物质等如何导致白血病,机制并未完全清楚。细胞的增殖、分化和衰老死亡都是由基因决定的,显然细胞的恶性转化也必然与基因的某种改变相关联。现知动物和人类细胞以及某些种类的病毒株中都存在能诱导正常细胞恶性转化,并使其获得新生物特性的肿瘤基因,前者称为细胞癌基因(cell oncogene)或原癌基因,后者称为病毒癌基因(virus oncogene)。细胞癌基因原是正常基因的成员,他们在细胞增殖、分化、衰老死亡进程的一定时期起作用,并受内在机制的调节和节制,当这些基因异常激活转为肿瘤基因时,就具有了致癌活性。研究表明病毒癌基因并非是病毒本身固有的,而是...[详细]
儿童急性白血病的临床表现有共性,主要表现为贫血、皮肤黏膜或内脏出血倾向、发热及各种类型感染。与ALL不同的是M3型临床有更严重的出血倾向,在治疗前及刚开始治疗时易发生DIC,而M5型齿龈浸润较多见。除M4、M5以外,其他AML浸润中枢神经系统的机会比ALL少。 体格检查除不同程度面色苍白、出血点、紫癜外,半数以上病人有肝、脾、淋巴结不同程度肿大;皮肤、皮下组织浸润时扪及结节,眼眶部浸润时可有眼球突出,这些浸润性肿块(肿瘤部分)切面可因肿瘤细胞所含的髓过氧化酶作用而转化为绿色,因此又将其称为“绿色瘤”。
1.贫血和出血 贫血进行性加重,可出现心悸、耳鸣,溶血和不同程度的出血。M3型临床有更严重的出血倾向,在治疗前及刚开始治疗时易发生DIC。可发生皮下血肿,眼底视网膜出血,导致视力减退。消化道和泌尿道出血。颅内出血时、颅内压增高,表现为头痛、呕吐、抽搐和昏迷等。消化道和颅内出血可致患儿死亡。 2.感染 常并发感染,易扩散为败血症;常见的感染部位有呼吸系统、皮肤疖肿、肠道炎症,肛周炎等, 可发生鹅口疮、肛周真菌症、真菌性肠炎和深部真菌感染等。 3.白血病细胞浸润 可并发骨髓衰竭和全身组织器官被浸润,并发绿色瘤,肝脾、淋巴结肿大;上腔静脉综合征;关节肿痛,使行动受碍;中枢神经系统浸润时可并发中枢神经系统白血病,可表现为颅内压增高,有头痛、呕吐、视盘水肿所致视力模糊,也可引起面瘫等脑神经损害症,甚至发生癫痫样发作,意识障碍等;两侧腮腺无痛性增大;睾丸白血病;肾脏明显肿大;皮肤、胃肠道、肺、胸膜和心脏浸润时,引起相应脏器功能障碍的症状等。[收起]
1.贫血和出血 贫血进行性加重,可出现心悸、耳鸣,溶血和不同程度的出血。M3型临床有更严重的出血倾向,在治疗前及刚开始治疗时易发生DIC。可发生皮下血肿,眼底视网膜出血,导致视力减退。消化道和泌尿道出血。颅内出血时、颅内压增高,表现为头痛、呕吐、抽搐和昏迷等。消化道和颅内出血可致患儿死亡。 2.感染 常并发感染,易扩散为败血症;常见的感染部位有呼吸系统、皮肤疖肿、肠道炎症,肛周炎等, 可发生鹅口疮、肛周真菌症、真菌性肠炎和深部真菌感染等。 3.白血病细胞浸润 可并发骨髓衰竭和全身组织器官被浸润,并发绿色瘤,肝脾、淋巴结肿大;上腔静脉综合征;关节肿痛,使行动受碍;中枢神...[详细]
1.血象 外周血检查表现为红细胞、血红蛋白(Hb)不同程度的下降;白细胞计数(WBC)约半数以上明显增高,余可正常或降低,此时又称低增生性白血病。白细胞升高者外周血中易见到白血病细胞,是诊断白血病的有力证据。白细胞降低者血中不易见到白血病细胞,又称为非白血性白血病(aleukemic leukemia)。有报告1024例ALL患儿的血象如下:①白细胞<10×109/L者占34%,(10~24)×109/L占25%,(25~49)×109/L占22%,>50×109/L者占19%。②Hb水平<70g/L占44%,70~110g/L占43%,>110g/L占14%。③BPC≤20×109/L占29%,(20~49)×109/L占23%,(50~99)×109/L占20%,≥100×109/L占29%。 2.骨髓象 初诊急白患儿的骨髓象绝大部分增生明显活跃或极度活跃,少数病例显示增生低下称为低增生性白血病,后者预后较佳。至今为止骨髓象仍是诊断急白的最确切依据,其中原始加幼稚细胞的比例≥30%方可诊断,ANLL还要去掉红系再计算这个比例。由于骨髓中正常造血细胞的分化成熟障碍,代之而起的是大量停滞于某个阶段的白血病细胞,因之出现成熟过程中的一至多个阶段缺如,称为“裂孔”现象。AML中尤其是原幼粒细胞中,常可见到棒状的Auer小体,在与ALL的鉴别中有一定价值。近年发现3,3-二基联苯胺染色的AML细胞中可见到棒状或纺锤形phi小体,50%以上的急粒中可检出,有助于鉴别诊断。 3.其他 白血病的免疫学、细胞化学、细胞遗传学检查前已述及,透射电镜等的使用可帮助诊断M7和急性未分化性白血病,末端脱氧核苷酸转移酶(terminal deoxynucleotidyl transferase,TdT)在B-ALL和AML中明显减低,在T-ALL、C-ALL Pre-B-ALL中均明显增高,因而有一定鉴别意义。[收起]
1.血象 外周血检查表现为红细胞、血红蛋白(Hb)不同程度的下降;白细胞计数(WBC)约半数以上明显增高,余可正常或降低,此时又称低增生性白血病。白细胞升高者外周血中易见到白血病细胞,是诊断白血病的有力证据。白细胞降低者血中不易见到白血病细胞,又称为非白血性白血病(aleukemic leukemia)。有报告1024例ALL患儿的血象如下:①白细胞<10×109/L者占34%,(10~24)×109/L占25%,(25~49)×109/L占22%,>50×109/L者占19%。②Hb水平<70g/L占44%,70~110g/L占43%,>110g/L占14%。③BPC≤20×109/L占2...[详细]
1.胸片检查 急白的X线多为非特异性,胸片常有肺门淋巴结肿大,白血病浸润肺时可见斑状影。T-ALL常有纵隔肿块影。 2.骨X线片检查 常显示骨质疏松和脱钙,有时有局灶性溶骨和层状骨膜反应征,长骨干骨骺端出现密度降低的横纹带称为白血病线。
1.以下情况应考虑本病诊断 (1)对不明原因的贫血、出血、发热和不能以感染完全解释的发热,以及多脏器浸润症状表现者应考虑本病诊断。 (2)对体格检查中发现有与出血程度不相符的贫血、肝、脾、淋巴结肿大者,尤其有腮腺、睾丸和软组织浸润肿大者,以及伴有骨、关节痛明显者应考虑本病的诊断。 (3)外周血发现≥2个系列异常或见有幼稚细胞者应考虑到本病的可能,进一步作骨髓涂片检查。 2.白血病诊断应包括以下3个内容 细胞形态学、免疫表型和细胞遗传学,随着发展还应包括基因型的分析。 (1)骨髓细胞形态学:当临床怀疑白血病时必须进行骨髓涂片做形态学、组织化学染色检查才能明确诊断。骨髓涂片显示常为高度增生,幼稚细胞≥30%,在30%~100%,约4/5病人在形态学和组织化学染色检查后能作出明确的形态分型诊断,另1/5病人需进行免疫表型和细胞遗传学分析来进一步鉴别AML和ALL。AML各型中组织化学染色特征见表1。 (2)免疫表型:当骨髓造血干细胞逐步分化成熟时可表达与特定细胞系和分化阶段相关的免疫表型,在细胞形态学和组织化学染色结果不一致时,免疫表型对诊断起重要作用。90%的AML病人中至少表达CD33、CD13、CD15、CD11b和CD36中的一个。有些髓系抗原也表达于幼稚淋巴细胞上,因此也不能仅根据免疫表型来作诊断,4%~25%的ALL可表达至少1个髓系抗原,11%~28%的AML,同时表达淋巴系抗原。 (3)细胞遗传学:AML中常见的并有特征性的染色体异常有t(8;21)、t(3;21),常见于M2;t(15;17)、t(11;17),常见于M3;inv(16)常见于M4Eo。[收起]
1.以下情况应考虑本病诊断 (1)对不明原因的贫血、出血、发热和不能以感染完全解释的发热,以及多脏器浸润症状表现者应考虑本病诊断。 (2)对体格检查中发现有与出血程度不相符的贫血、肝、脾、淋巴结肿大者,尤其有腮腺、睾丸和软组织浸润肿大者,以及伴有骨、关节痛明显者应考虑本病的诊断。 (3)外周血发现≥2个系列异常或见有幼稚细胞者应考虑到本病的可能,进一步作骨髓涂片检查。 2.白血病诊断应包括以下3个内容 细胞形态学、免疫表型和细胞遗传学,随着发展还应包括基因型的分析。 (1)骨髓细胞形态学:当临床怀疑白血病时必须进行骨髓涂片做形态学、组织化学染...[详细]
AML治疗原则是有效药物联合强化疗、注意诱导缓解及继续治疗中的药物剂量强度和给药时间强度,小剂量长期维持治疗对AML的无病生存率无影响。治疗合理时,5年无病生存率为30%~45%。 1.诱导治疗 国际常用的诱导治疗方案为DA方案,即柔红霉素40mg/m2,1次/d×3天;阿糖胞苷(Ara-C)75~100mg/次,每12小时1次×7天。我国特有的三尖杉碱对儿童AML也有效,与阿糖胞苷(Ara-C)联合为HA方案,即(H)三尖杉碱4mg/m2,1次/d×9天;阿糖胞苷(Ara-C)75~100mg/次,每12小时1次×7天,其诱导缓解率与DA方案相似。80%~85%初治病人在1~2个疗程后获得缓解。 2.继续化疗 AML在缓解后可再继续用原方案1~2疗程作为巩固治疗。从目前进展来说,包含大剂量阿糖胞苷(Ara-C)的方案可改善AML的预后。常用方法为阿糖胞苷(Ara-C)每次2g/m2,每12小时1次×6次;联合柔红霉素40mg/m2×2天或依托泊苷(VP-16)160mg/m2×2天,每2~3周1个疗程,在巩固治疗之后连续3个疗程作为强化治疗。与AML不同,ALL需较长期的低剂量维持化疗,但在AML中需连续的骨髓抑制性化疗,持续化疗至12个月左右即可停药,延长化疗时间并不改善预后,持续化疗方案可用HA、DA、大剂量阿糖胞苷(Ara-C)交替,注意整个治疗期蒽环类抗肿瘤类药物累积剂量,一般控制在350mg/m2以下。具体疗程安排见图2。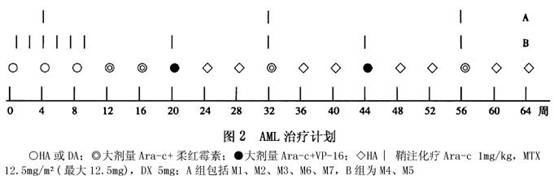 维A酸(全反式维A酸)对M3有效,可诱导其分化成熟,60%~70%病人在单用维A酸后可获得缓解,但如不加用化疗,仍复发。目前主张对M3病人用3~10天维A酸后起用AML诱导化疗,并按AML继续化疗。维A酸的应用可明显减少化疗诱导的DIC发生率,化疗联合维A酸的治疗方式对无病生存率的影响优于单用化疗,维A酸在缓解后间断给药,如每2~3个月给7~14天,化疗仍按AML进行。 3.中枢神经系统浸润预防 对M4、M5需与ALL相仿的鞘内化疗作中枢神经系统浸润预防,用法见图2中所示。对其他AML是否需预防尚有争论。 4.骨髓移植 AML预后较ALL明显差,特别是有高危因素者更差,因此对这部分病人如有HLA相合的相关家属供体应考虑作异体基因造血干细胞移植。自身造血干细胞移植是否有效尚有争论,多数报告为与常规化疗者无差异。 5.复发与再治 AML复发后再治困难,尤其是治疗中复发者,如能获得再次缓解,应争取在短期内作异体基因造血干细胞移植,因再次缓解时间常短暂。[收起]
AML治疗原则是有效药物联合强化疗、注意诱导缓解及继续治疗中的药物剂量强度和给药时间强度,小剂量长期维持治疗对AML的无病生存率无影响。治疗合理时,5年无病生存率为30%~45%。 1.诱导治疗 国际常用的诱导治疗方案为DA方案,即柔红霉素40mg/m2,1次/d×3天;阿糖胞苷(Ara-C)75~100mg/次,每12小时1次×7天。我国特有的三尖杉碱对儿童AML也有效,与阿糖胞苷(Ara-C)联合为HA方案,即(H)三尖杉碱4mg/m2,1次/d×9天;阿糖胞苷(Ara-C)75~100mg/次,每12小时1次×7天,其诱导缓解率与DA方案相似。80%~85%初治病人在1~2...[详细]
维A酸(全反式维A酸)对M3有效,可诱导其分化成熟,60%~70%病人在单用维A酸后可获得缓解,但如不加用化疗,仍复发。目前主张对M3病人用3~10天维A酸后起用AML诱导化疗,并按AML继续化疗。维A酸的应用可明显减少化疗诱导的DIC发生率,化疗联合维A酸的治疗方式对无病生存率的影响优于单用化疗,维A酸在缓解后间断给药,如每2~3个月给7~14天,化疗仍按AML进行。 3.中枢神经系统浸润预防 对M4、M5需与ALL相仿的鞘内化疗作中枢神经系统浸润预防,用法见图2中所示。对其他AML是否需预防尚有争论。 4.骨髓移植 AML预后较ALL明显差,特别是有高危因素者更差,因此对这部分病人如有HLA相合的相关家属供体应考虑作异体基因造血干细胞移植。自身造血干细胞移植是否有效尚有争论,多数报告为与常规化疗者无差异。 5.复发与再治 AML复发后再治困难,尤其是治疗中复发者,如能获得再次缓解,应争取在短期内作异体基因造血干细胞移植,因再次缓解时间常短暂。[收起]
AML治疗原则是有效药物联合强化疗、注意诱导缓解及继续治疗中的药物剂量强度和给药时间强度,小剂量长期维持治疗对AML的无病生存率无影响。治疗合理时,5年无病生存率为30%~45%。 1.诱导治疗 国际常用的诱导治疗方案为DA方案,即柔红霉素40mg/m2,1次/d×3天;阿糖胞苷(Ara-C)75~100mg/次,每12小时1次×7天。我国特有的三尖杉碱对儿童AML也有效,与阿糖胞苷(Ara-C)联合为HA方案,即(H)三尖杉碱4mg/m2,1次/d×9天;阿糖胞苷(Ara-C)75~100mg/次,每12小时1次×7天,其诱导缓解率与DA方案相似。80%~85%初治病人在1~2...[详细]
较为公认的影响AML预后的不良因素,有以下几点: 1.起病时白细胞总数>100×109/L。 2.AML为第二肿瘤。 3.细胞遗传学示单倍体7,及由MDS转化而来的AML。 除此以外,巨脾、M4或M5、1个疗程未获缓解也被认为是影响预后的不良因素。
1.避免接触有害因素 避免接触有害化学物质、电离辐射等引起白血病的因素,接触毒物或放射性物质时,应加强各种防护措施;避免环境污染,尤其是室内环境污染;注意合理用药,慎用细胞毒药物等。 2.大力开展防治各种感染性疾病,尤其是病毒感染性疾病,做好预防接种。 3.做好优生工作,防止某些先天性疾病,如21-三体、范可尼贫血等。加强体育锻炼,注意饮食卫生,保持心情舒畅,劳逸结合,增强机体抵抗力。

 维A酸(全反式维A酸)对M3有效,可诱导其分化成熟,60%~70%病人在单用维A酸后可获得缓解,但如不加用化疗,仍复发。目前主张对M3病人用3~10天维A酸后起用AML诱导化疗,并按AML继续化疗。维A酸的应用可明显减少化疗诱导的DIC发生率,化疗联合维A酸的治疗方式对无病生存率的影响优于单用化疗,维A酸在缓解后间断给药,如每2~3个月给7~14天,化疗仍按AML进行。 3.中枢神经系统浸润预防 对M4、M5需与ALL相仿的鞘内化疗作中枢神经系统浸润预防,用法见图2中所示。对其他AML是否需预防尚有争论。 4.骨髓移植 AML预后较ALL明显差,特别是有高危因素者更差,因此对这部分病人如有HLA相合的相关家属供体应考虑作异体基因造血干细胞移植。自身造血干细胞移植是否有效尚有争论,多数报告为与常规化疗者无差异。 5.复发与再治 AML复发后再治困难,尤其是治疗中复发者,如能获得再次缓解,应争取在短期内作异体基因造血干细胞移植,因再次缓解时间常短暂。
维A酸(全反式维A酸)对M3有效,可诱导其分化成熟,60%~70%病人在单用维A酸后可获得缓解,但如不加用化疗,仍复发。目前主张对M3病人用3~10天维A酸后起用AML诱导化疗,并按AML继续化疗。维A酸的应用可明显减少化疗诱导的DIC发生率,化疗联合维A酸的治疗方式对无病生存率的影响优于单用化疗,维A酸在缓解后间断给药,如每2~3个月给7~14天,化疗仍按AML进行。 3.中枢神经系统浸润预防 对M4、M5需与ALL相仿的鞘内化疗作中枢神经系统浸润预防,用法见图2中所示。对其他AML是否需预防尚有争论。 4.骨髓移植 AML预后较ALL明显差,特别是有高危因素者更差,因此对这部分病人如有HLA相合的相关家属供体应考虑作异体基因造血干细胞移植。自身造血干细胞移植是否有效尚有争论,多数报告为与常规化疗者无差异。 5.复发与再治 AML复发后再治困难,尤其是治疗中复发者,如能获得再次缓解,应争取在短期内作异体基因造血干细胞移植,因再次缓解时间常短暂。 浙公网安备
33010902000463号
浙公网安备
33010902000463号