多囊卵巢综合征(polycystic ovarian syndrome,PCOS)是育龄妇女较常见的内分泌症候群。1935年,Stein与Leventhal首先描述双侧卵巢肿大者伴不孕、多毛与肥胖等表现,称为Stein-Leventhal综合征。随着临床研究的深入,组织学上具有多囊卵巢伴无排卵和(或)多毛症的临床症候群范围不断扩大。1963年,Goldziether总结187篇共1079例PCOS资料,发现其中有许多非典型病例,如无多毛,甚至有排卵功能。随着检测技术的发展,认识到多囊卵巢并非一种独特的疾病,而是一种多病因、表现极不均一的临床综合征。
PCOS的病因尚不清楚。一般认为与下丘脑-垂体-卵巢轴功能失常、肾上腺功能紊乱、遗传、代谢等因素有关。少数PCOS患者有性染色体或常染色体异常,有些还有家族史。近来发现某些基因(如CYP11A、胰岛素基因的VNTR)与PCOS发生有关,进一步肯定了遗传因素在PCOS发病中的作用。
PCOS的发病机制复杂,已被公认的事实是:①高LH伴正常或低水平的FSH;②雄激素增多;③恒定的雌激素水平(E1比E2高);④胰岛素抵抗(高胰岛素血症);⑤卵巢组织形态学上有多个囊性卵泡和间质增生。 1.促性腺激素释放异常 PCOS患者的血LH升高,而FSH正常或降低,LH/FSH≥2~3,静脉注射GnRH后LH可出现过度反应,认为可能原发于下丘脑-垂体功能失调。在下丘脑中多巴胺能和阿片肽能神经对GnRH神经元的抑制作用失控,可导致LH分泌增加。但更可能是雌激素的反馈抑制异常所致。非周期性的腺外转化而来的雌激素(雌酮E1)将导致对LH分泌的正反馈和对FSH分泌的负反馈抑制。LH刺激卵泡细胞增生,产生大量雄激素,雄激素不能全部转化成雌激素,进一步增加腺外芳香化E1的生成。过多雄激素使卵泡闭锁、卵巢包膜纤维化和包膜增厚。由于缺乏月经周期中期的LH峰值,出现排卵障碍(图1)。此外,有人发现PCOS患者的卵巢也可能分泌“抑制素”,抑制FSH的分泌,影响卵泡的发育成熟,出现较多囊状卵泡,近年发现高胰岛素血症和增高的IGF也可使LH分泌增多。 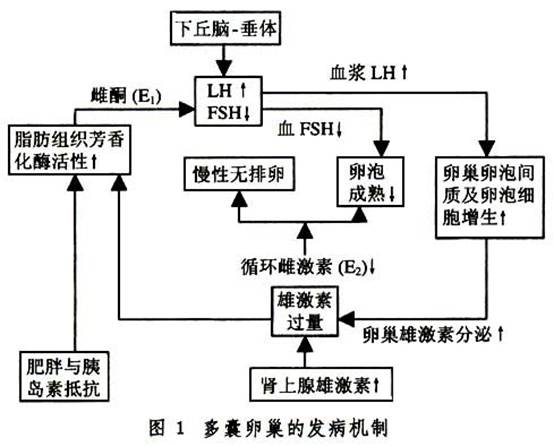 2.雄激素过多 在PCOS中,几乎所有的雄激素生成均增多。而性激素结合球蛋白(SHBG)减少,游离雄激素增多,活性增强。至于过多的雄激素来源于卵巢或肾上腺众说不一。大剂量GnRH激动剂可降低促性腺激素,雄烯二酮和睾酮减少,而对来源于肾上腺的DHEAS无影响。据报道大约70%的PCOS患者为卵巢源性雄激素所致:①由于类固醇激素所需酶系功能紊乱,如芳香化酶缺乏,3β-醇甾脱氢酶不足或活性下降,P45OC17A调节异常,雌激素合成障碍,大量雄激素在外周(脂肪、肝、肾内)转换为雌酮。也有人认为卵巢发育不充分使芳香化酶的活性下降。②LH脉冲频率及振幅升高,刺激卵泡膜细胞及间质细胞增生和雄激素的生成。过多的雄激素促使卵泡闭锁,卵巢粒层细胞早期黄素化,生长停止,不能排卵,形成PCOS。 本病多发生在青春期月经初潮后,推测可能起因于性成熟前期,肾上腺功能失调,持续分泌过多雄激素。此外,在应用地塞米松前后测定卵巢和肾上腺静脉血中的各种雄激素水平,其结果支持卵巢和肾上腺是PCOS过多雄激素的共同来源,发现50%PCOS患者有肾上腺源性雄激素增多。 3.雌酮过多 PCOS妇女用孕酮等药物有撤退性子宫出血,服氯底酚胺可导致卵泡成熟排卵,月经来潮,这提示PCOS患者不但雄激素水平高,而且雌激素也增多。体内活性雌激素包括雌二醇(E2)和雌酮(E1),E2主要来源于卵巢,E1则来自卵巢、肾上腺及周围组织的转换。PCOS患者非周期性E1明显增多,E1/F2比率增高(正常E1/F2≤1),特别是肥胖者的脂肪多,芳香化酶活性高,外周组织转换增多,E1水平可更高,而且来源于外周组织的E1不受垂体促性腺激素的调节,无周期性变化。持续高水平的雌激素对下丘脑-垂体的反馈调节是不正常的。 4.细胞色素P450C17A调节失常 PCOS主要缺陷是下丘脑-垂体接受异常的反馈信号。这可能与卵巢和肾上腺本身的自分泌、旁分泌调节机制障碍有关。PCOS患者常伴17-羟孕酮(17-OHP)升高,这是由于卵泡膜细胞内或肾上腺网状带内P450C17A的调节机制失常所致。P450C17A具有17-羟化酶和17,20-链裂酶的双重活性,在?4将孕酮转换为17-OHP和雄烯二酮,在?5将孕烯醇酮衍变为17-羟孕烯醇酮和DHEA。 17-羟孕酮既是肾上腺合成皮质醇的重要前体物质.也是卵巢合成性激素特别是雄激素的重要前体。若给予PCOS患者GnRH-A或HCG(特别在用地塞米松抑制后),17-羟孕酮、雄烯二酮明显升高;而ACTH兴奋试验又能促使肾上腺的DHEA与17-OHP同时增多,提示卵巢和肾上腺网状带的P450C17A活性增高。因此,P450C17A活性调节异常是肾上腺和卵巢雄激素过量分泌的重要原因。但为什么会出现类固酮合成的调节异常尚不清楚。胰岛素/IGFs系统可刺激卵巢和肾上腺P450C17A mRNA表达及其活性。此外,CYP11A的侧链裂解酶基因编码区与产生过多雄激素有关。 5.胰岛素抵抗与高胰岛素血症 PCOS患者不论有无肥胖,多有不同程度的胰岛素抵抗与高胰岛素血症。近期发现大约有半数PCOS患者的发病与胰岛素受体丝氨酸磷酸化缺陷有关。因而认为胰岛素在其发病中占有重要地位。胰岛素与IGF-1通过IGF-1受体作用于卵泡膜细胞,促使雄烯二酮和睾酮合成。近年的研究发现,垂体邻近部位有胰岛素受体,或者同时存在的高IGF-1血症可促进LH刺激的卵泡膜细胞增生,导致雄激素过多和卵泡过早闭锁(图2)。Hasegawa用胰岛素增敏剂Troglitazone治疗PCOS,可使胰岛素水平降低,LH和雄激素水平相应降低也支持这一观点。胰岛素升高对调节SHBG的代谢有重要作用,可使肝脏SHBG生成减少,游离睾酮升高。此外,胰岛素受体丝氨酸磷酸化可抑制胰岛素受体活性,促进P450C17A的17,20-链裂酶活性。近年对位于染色体11pl5.5的胰岛素基因的5'-端可变数串联重复顺序(VNTR)的研究发现,胰岛素基因的VNTR是PCOS的一个主要易感位点(特别是排卵性PCOS)。说明胰岛素VNTR多态性是PCOS的遗传学因素。
2.雄激素过多 在PCOS中,几乎所有的雄激素生成均增多。而性激素结合球蛋白(SHBG)减少,游离雄激素增多,活性增强。至于过多的雄激素来源于卵巢或肾上腺众说不一。大剂量GnRH激动剂可降低促性腺激素,雄烯二酮和睾酮减少,而对来源于肾上腺的DHEAS无影响。据报道大约70%的PCOS患者为卵巢源性雄激素所致:①由于类固醇激素所需酶系功能紊乱,如芳香化酶缺乏,3β-醇甾脱氢酶不足或活性下降,P45OC17A调节异常,雌激素合成障碍,大量雄激素在外周(脂肪、肝、肾内)转换为雌酮。也有人认为卵巢发育不充分使芳香化酶的活性下降。②LH脉冲频率及振幅升高,刺激卵泡膜细胞及间质细胞增生和雄激素的生成。过多的雄激素促使卵泡闭锁,卵巢粒层细胞早期黄素化,生长停止,不能排卵,形成PCOS。 本病多发生在青春期月经初潮后,推测可能起因于性成熟前期,肾上腺功能失调,持续分泌过多雄激素。此外,在应用地塞米松前后测定卵巢和肾上腺静脉血中的各种雄激素水平,其结果支持卵巢和肾上腺是PCOS过多雄激素的共同来源,发现50%PCOS患者有肾上腺源性雄激素增多。 3.雌酮过多 PCOS妇女用孕酮等药物有撤退性子宫出血,服氯底酚胺可导致卵泡成熟排卵,月经来潮,这提示PCOS患者不但雄激素水平高,而且雌激素也增多。体内活性雌激素包括雌二醇(E2)和雌酮(E1),E2主要来源于卵巢,E1则来自卵巢、肾上腺及周围组织的转换。PCOS患者非周期性E1明显增多,E1/F2比率增高(正常E1/F2≤1),特别是肥胖者的脂肪多,芳香化酶活性高,外周组织转换增多,E1水平可更高,而且来源于外周组织的E1不受垂体促性腺激素的调节,无周期性变化。持续高水平的雌激素对下丘脑-垂体的反馈调节是不正常的。 4.细胞色素P450C17A调节失常 PCOS主要缺陷是下丘脑-垂体接受异常的反馈信号。这可能与卵巢和肾上腺本身的自分泌、旁分泌调节机制障碍有关。PCOS患者常伴17-羟孕酮(17-OHP)升高,这是由于卵泡膜细胞内或肾上腺网状带内P450C17A的调节机制失常所致。P450C17A具有17-羟化酶和17,20-链裂酶的双重活性,在?4将孕酮转换为17-OHP和雄烯二酮,在?5将孕烯醇酮衍变为17-羟孕烯醇酮和DHEA。 17-羟孕酮既是肾上腺合成皮质醇的重要前体物质.也是卵巢合成性激素特别是雄激素的重要前体。若给予PCOS患者GnRH-A或HCG(特别在用地塞米松抑制后),17-羟孕酮、雄烯二酮明显升高;而ACTH兴奋试验又能促使肾上腺的DHEA与17-OHP同时增多,提示卵巢和肾上腺网状带的P450C17A活性增高。因此,P450C17A活性调节异常是肾上腺和卵巢雄激素过量分泌的重要原因。但为什么会出现类固酮合成的调节异常尚不清楚。胰岛素/IGFs系统可刺激卵巢和肾上腺P450C17A mRNA表达及其活性。此外,CYP11A的侧链裂解酶基因编码区与产生过多雄激素有关。 5.胰岛素抵抗与高胰岛素血症 PCOS患者不论有无肥胖,多有不同程度的胰岛素抵抗与高胰岛素血症。近期发现大约有半数PCOS患者的发病与胰岛素受体丝氨酸磷酸化缺陷有关。因而认为胰岛素在其发病中占有重要地位。胰岛素与IGF-1通过IGF-1受体作用于卵泡膜细胞,促使雄烯二酮和睾酮合成。近年的研究发现,垂体邻近部位有胰岛素受体,或者同时存在的高IGF-1血症可促进LH刺激的卵泡膜细胞增生,导致雄激素过多和卵泡过早闭锁(图2)。Hasegawa用胰岛素增敏剂Troglitazone治疗PCOS,可使胰岛素水平降低,LH和雄激素水平相应降低也支持这一观点。胰岛素升高对调节SHBG的代谢有重要作用,可使肝脏SHBG生成减少,游离睾酮升高。此外,胰岛素受体丝氨酸磷酸化可抑制胰岛素受体活性,促进P450C17A的17,20-链裂酶活性。近年对位于染色体11pl5.5的胰岛素基因的5'-端可变数串联重复顺序(VNTR)的研究发现,胰岛素基因的VNTR是PCOS的一个主要易感位点(特别是排卵性PCOS)。说明胰岛素VNTR多态性是PCOS的遗传学因素。  6.肥胖 PCOS伴肥胖者(BMI≥25)占20%~60%。体脂分布不均匀。现知脂肪组织是类固醇激素的重要代谢场所,脂肪组织中的芳香化酶将外周雄激素转换为E1和E2。研究证实,雄烯二酮转换为E1的量与脂肪组织总量相关,高雄激素血症时SHBG下降,游离E2增加。雌激素使脂肪细胞生长、增殖。不同的内分泌环境能造成不同的肥胖体态,雄激素升高表现为上身肥胖(即男性型肥胖),而雌激素增多者为下身肥胖(即女性型肥胖)。体重增加常伴血胰岛素升高和SHBG及IGFBP下降,从而使游离性激素和IGF-1增多。这类患者常伴有糖耐量异常或2型糖尿病。 近来,Rouru等提出肥胖-瘦素-NPY轴可能是部分PCOS患者下丘脑-垂体-LH过度分泌的病因,即肥胖妇女的瘦素分泌增多,后者抑制下丘脑NPYmRNA表达和NPY的分泌,解除NPY对LH的抑制,促使LH大量释放。 7.高泌乳素血症 高泌乳素血症与PCOS的关系尚待进一步研究。[收起]
PCOS的发病机制复杂,已被公认的事实是:①高LH伴正常或低水平的FSH;②雄激素增多;③恒定的雌激素水平(E1比E2高);④胰岛素抵抗(高胰岛素血症);⑤卵巢组织形态学上有多个囊性卵泡和间质增生。 1.促性腺激素释放异常 PCOS患者的血LH升高,而FSH正常或降低,LH/FSH≥2~3,静脉注射GnRH后LH可出现过度反应,认为可能原发于下丘脑-垂体功能失调。在下丘脑中多巴胺能和阿片肽能神经对GnRH神经元的抑制作用失控,可导致LH分泌增加。但更可能是雌激素的反馈抑制异常所致。非周期性的腺外转化而来的雌激素(雌酮E1)将导致对LH分泌的正反馈和对FSH分泌的负反馈抑制。LH刺激卵...[详细]
6.肥胖 PCOS伴肥胖者(BMI≥25)占20%~60%。体脂分布不均匀。现知脂肪组织是类固醇激素的重要代谢场所,脂肪组织中的芳香化酶将外周雄激素转换为E1和E2。研究证实,雄烯二酮转换为E1的量与脂肪组织总量相关,高雄激素血症时SHBG下降,游离E2增加。雌激素使脂肪细胞生长、增殖。不同的内分泌环境能造成不同的肥胖体态,雄激素升高表现为上身肥胖(即男性型肥胖),而雌激素增多者为下身肥胖(即女性型肥胖)。体重增加常伴血胰岛素升高和SHBG及IGFBP下降,从而使游离性激素和IGF-1增多。这类患者常伴有糖耐量异常或2型糖尿病。 近来,Rouru等提出肥胖-瘦素-NPY轴可能是部分PCOS患者下丘脑-垂体-LH过度分泌的病因,即肥胖妇女的瘦素分泌增多,后者抑制下丘脑NPYmRNA表达和NPY的分泌,解除NPY对LH的抑制,促使LH大量释放。 7.高泌乳素血症 高泌乳素血症与PCOS的关系尚待进一步研究。[收起]
PCOS的发病机制复杂,已被公认的事实是:①高LH伴正常或低水平的FSH;②雄激素增多;③恒定的雌激素水平(E1比E2高);④胰岛素抵抗(高胰岛素血症);⑤卵巢组织形态学上有多个囊性卵泡和间质增生。 1.促性腺激素释放异常 PCOS患者的血LH升高,而FSH正常或降低,LH/FSH≥2~3,静脉注射GnRH后LH可出现过度反应,认为可能原发于下丘脑-垂体功能失调。在下丘脑中多巴胺能和阿片肽能神经对GnRH神经元的抑制作用失控,可导致LH分泌增加。但更可能是雌激素的反馈抑制异常所致。非周期性的腺外转化而来的雌激素(雌酮E1)将导致对LH分泌的正反馈和对FSH分泌的负反馈抑制。LH刺激卵...[详细]
1.月经异常 月经稀少、闭经,少数可表现为功能性子宫出血。多发生在青春期,为初潮后不规则月经的继续,有时伴痛经。 2.多毛 较常见,发生率可达69%。由于雄激素升高,可见上唇、下颌、胸、背、小腹正中部、大腿上部两侧及肛周的毳毛增粗、增多,但多毛的程度与雄激素水平不成比例(受体数、雌激素、SHBG及毛囊对雄激素的敏感性等多种因素影响)。同时可伴痤疮、面部皮脂分泌过多、声音低粗、阴蒂肥大、出现喉结等男性化征象。 3.不孕 由于长期不排卵,患者多合并不孕症,有时可有偶发性排卵或流产,发生率可达74%。 4.肥胖 体重超过20%以上,体重指数≥25者占30%~60%。肥胖多集中于上身,腰/臀比例>0.85。多自青春期开始,随年龄增长而逐渐加重。 5.卵巢增大 少数病人可通过一般妇科检查触及增大、质地坚韧的卵巢,大多需辅助检查确定。 6.雌激素作用 所有病人都表现为雌激素作用良好。检查时,可见宫颈黏液量多。持续、大量雌激素作用可出现内膜增生过快,非典型性增生,甚至癌变。 多囊卵巢综合征的临床特征见表1。 [收起]
1.月经异常 月经稀少、闭经,少数可表现为功能性子宫出血。多发生在青春期,为初潮后不规则月经的继续,有时伴痛经。 2.多毛 较常见,发生率可达69%。由于雄激素升高,可见上唇、下颌、胸、背、小腹正中部、大腿上部两侧及肛周的毳毛增粗、增多,但多毛的程度与雄激素水平不成比例(受体数、雌激素、SHBG及毛囊对雄激素的敏感性等多种因素影响)。同时可伴痤疮、面部皮脂分泌过多、声音低粗、阴蒂肥大、出现喉结等男性化征象。 3.不孕 由于长期不排卵,患者多合并不孕症,有时可有偶发性排卵或流产,发生率可达74%。 4.肥胖 体重超过20%以上,体重指数≥25者占30%~60...[详细]
[收起]
1.月经异常 月经稀少、闭经,少数可表现为功能性子宫出血。多发生在青春期,为初潮后不规则月经的继续,有时伴痛经。 2.多毛 较常见,发生率可达69%。由于雄激素升高,可见上唇、下颌、胸、背、小腹正中部、大腿上部两侧及肛周的毳毛增粗、增多,但多毛的程度与雄激素水平不成比例(受体数、雌激素、SHBG及毛囊对雄激素的敏感性等多种因素影响)。同时可伴痤疮、面部皮脂分泌过多、声音低粗、阴蒂肥大、出现喉结等男性化征象。 3.不孕 由于长期不排卵,患者多合并不孕症,有时可有偶发性排卵或流产,发生率可达74%。 4.肥胖 体重超过20%以上,体重指数≥25者占30%~60...[详细]
1.肿瘤 持续的、无周期性的、相对偏高的雌激素水平和升高的E1与E1/E2比值对子宫内膜的刺激,又无孕激素抵抗,使子宫内膜癌和乳腺癌发病率增加。 2.心血管疾病 血脂代谢紊乱,易引起动脉粥样硬化,导致冠心病、高血压等。 3.糖尿病 胰岛素抵抗状态和高胰岛素血症、肥胖,易发展为隐性糖尿病或糖尿病。 痤疮:由于多毛所致面部皮脂分泌过多。 不孕症:由于闭经不排卵所致。
1.LH/FSH 血LH与FSH比值与浓度均异常,呈非周期性分泌,大多数患者LH增高,而FSH相当于早期卵泡期水平,LH/FSH≥2.5~3。不少学者认为LH/FSH比例增加是PCOS的特征。 2.雄性类固醇 雄激素过多,睾酮、雄烯二酮、DHEA、DHEAS水平均可增高。 3.雌性类固醇 雌酮与雌激素异常,恒定的雌激素水平,E2水平波动小,无正常的月经周期性变化,E1水平增加,E1/E2>1。 4.PRL PCOS时可轻度升高,但因高泌乳素血症可出现类PCOS症状,应加以鉴别。 5.尿17-OHCS和17-KS 24h尿17-酮升高反映肾上腺雄激素分泌的增多。 6.地塞米松抑制试验 可抑制肾上腺性激素的分泌,服用地塞米松0.5mg,每6小时1次,共4天,服后取血样,如血清硫酸脱氢异雄酮或尿17-酮类固醇被抑制至正常水平,可排除肾上腺肿瘤或增生之可能。 7.绒毛膜促性腺激素(HCG)刺激试验 HCG可刺激卵巢合成雄激素,注射HCG可引起血浆雄激素水平升高。 8.促皮质素(ACTH)兴奋试验 ACTH兴奋试验可促肾上腺源性雄激素DHEA及尿17-KS增高。 通过HCG刺激试验、地塞米松抑制试验、ACTH兴奋试验可帮助鉴别雄激素升高的来源。 9.阴道脱落细胞成熟指数 是初步了解体内性激素状况的简易方法。睾酮过多的涂片往往出现3层细胞同时存在的片型,明显增高时3层细胞数几乎相等,但必须与炎症相区别。雌激素水平可以从表层细胞百分比来估计,但不能反映血液中激素的含量。 10.基础体温测定 判断有无排卵,排卵者呈双相型,无排卵者一般为单相型。[收起]
1.LH/FSH 血LH与FSH比值与浓度均异常,呈非周期性分泌,大多数患者LH增高,而FSH相当于早期卵泡期水平,LH/FSH≥2.5~3。不少学者认为LH/FSH比例增加是PCOS的特征。 2.雄性类固醇 雄激素过多,睾酮、雄烯二酮、DHEA、DHEAS水平均可增高。 3.雌性类固醇 雌酮与雌激素异常,恒定的雌激素水平,E2水平波动小,无正常的月经周期性变化,E1水平增加,E1/E2>1。 4.PRL PCOS时可轻度升高,但因高泌乳素血症可出现类PCOS症状,应加以鉴别。 5.尿17-OHCS和17-KS 24h尿17-酮升高反映肾上腺雄激素分泌的增多。 6.地塞米松抑制试验 可抑制肾上...[详细]
1.盆腔B超 卵巢增大,每平面至少有10个以上2~6mm直径的卵泡,主要分布在卵巢皮质的周边,少数散在于间质中,间质增多。 2.气腹摄片 双侧卵巢增大2~3倍,若雄激素的主要来源为肾上腺,则卵巢相对较小。 3.腹腔镜(或手术时) 见卵巢形态饱满、表面苍白平滑、包膜厚、有时可见其下有毛细血管网。因外表颜色呈珍珠样,俗称牡蛎卵巢,表面可见多个囊状卵泡。 4.经阴道的高分辨力的超声检查卵巢,使得PCOS的诊断有了突破。目前,有经验的医生做这项检查已成为诊断学基础。经阴道100%可探测多囊卵巢,而经腹部有30%的病人漏诊。对于未婚肥胖的患者可应用肛门超声来检测。1986年Adams首先报道PCOS患者卵巢的超声特征为双侧卵巢内均有8个以上直径<10mm的卵泡,沿周边排列,伴有中央间质区增大。多囊卵巢通常是增大的,但也有正常大小的多囊卵巢。PCOS患者的超声相也可以是正常的。 5.CT、MRI也可用于卵巢形态的检查。[收起]
1.盆腔B超 卵巢增大,每平面至少有10个以上2~6mm直径的卵泡,主要分布在卵巢皮质的周边,少数散在于间质中,间质增多。 2.气腹摄片 双侧卵巢增大2~3倍,若雄激素的主要来源为肾上腺,则卵巢相对较小。 3.腹腔镜(或手术时) 见卵巢形态饱满、表面苍白平滑、包膜厚、有时可见其下有毛细血管网。因外表颜色呈珍珠样,俗称牡蛎卵巢,表面可见多个囊状卵泡。 4.经阴道的高分辨力的超声检查卵巢,使得PCOS的诊断有了突破。目前,有经验的医生做这项检查已成为诊断学基础。经阴道100%可探测多囊卵巢,而经腹部有30%的病人漏诊。对于未婚肥胖的患者可应用肛门超声来检测。1986年Adams首先报道PCOS患者...[详细]
1.临床诊断 初潮后多年月经仍不规则、月经稀少和(或)闭经,同时伴肥胖与多毛、婚后不孕等,应疑诊PCOS。典型病例具有上述各种症状及体征,即月经失调、多毛、痤疮、肥胖、不孕等。非典型病例可表现为:①单纯性闭经不伴有肥胖、多毛及卵巢肿大,排除其他各种疾病,而孕酮试验阳性者,仍应考虑为PCOS。②排卵型功能失调性出血。③月经异常合并多毛。④月经异常伴男性化症状,无明显肥胖。⑤功能失调性子宫出血伴不育。 对于不典型病例需详细询问有关病史,如起病年龄、生长发育情况,起病经过,用药史,家族史,个人生活习惯,既往有无全身性疾病。结合辅助检查,排除其他疾病,并经B超等检查明确诊断。 2.诊断标准 由于本病的异质性,诊断标准尚未统一,多数学者根据青春期发病、月经和排卵异常、多毛、血LH和(或)LH/FSH比值升高,结合一种雄激素水平过高,超声检查有多囊卵巢征象,排除其他类似疾病后,可确定本症的诊断。 日本妇产科学会生殖内分泌委员会于1993年提出PCOS诊断标准如下: (1)临床症状:①月经异常(闭经、月经稀发、无排卵月经等);②男性化(多毛、粉刺、声音低调、阴蒂肥大);③肥胖;④不孕。 (2)内分泌检查所见:①LH高值、FSH正常值;②注射GnRH后LH分泌增多,FSH分泌正常;③雌酮/雌二醇比值升高;④血中睾酮或雄烯二酮升高。 (3)卵巢所见:①B超见多个卵泡囊性变;②双合诊及B超见卵巢肿大;③腹腔镜见卵巢内膜肥厚及表面隆起;④镜下见卵泡膜细胞层肥厚增殖和间质增生。 以上的(1)、(2)、(3)项是必有的项目,3项均具备时可诊断为PCOS,其他项目做为参考,若所有必备和参考项目均具备,则为典型PCOS病例。 此外,亦有人提出的诊断标准如下:①临床症状:包括:A.闭经(60天以上);B.功能性子宫出血或持续无排卵(3个月以上);C.不孕;D.男性化体征;E.肥胖。②治疗性诊断:一度闭经,以氯米芬或加HCG疗法,于月经周期第5天开始,氯米芬50mg/d,连服5天,多可恢复排卵功能。无效时,可于停氯米芬后第2~4天加用HCH1000U,1次/d,共3天,治疗3个疗程以上仍未见排卵。③内分泌检查:包括:A.血中LH较高(20~50mU/ml)及GnRH过度反应,血FSH在正常范围或较低;B.血睾酮升高(60%以上);C.HMG(人绝经期促性腺激素)225U/d,用3天后,于用药的第6天尿中的雌激素呈过度增高反应(150μg/24h以上);D.地塞米松4mg/d,口服,于第5天的尿中11-去氧-17-酮类固醇增高(600μg/24h以上)。④卵巢形态(包括内镜所见):肉眼所见:A.无新鲜黄体形成;B.卵巢包膜增厚;C.卵巢增大;D.囊状肿大的卵泡并列于包膜下。组织所见:卵泡膜细胞及间质细胞黄素化。[收起]
1.临床诊断 初潮后多年月经仍不规则、月经稀少和(或)闭经,同时伴肥胖与多毛、婚后不孕等,应疑诊PCOS。典型病例具有上述各种症状及体征,即月经失调、多毛、痤疮、肥胖、不孕等。非典型病例可表现为:①单纯性闭经不伴有肥胖、多毛及卵巢肿大,排除其他各种疾病,而孕酮试验阳性者,仍应考虑为PCOS。②排卵型功能失调性出血。③月经异常合并多毛。④月经异常伴男性化症状,无明显肥胖。⑤功能失调性子宫出血伴不育。 对于不典型病例需详细询问有关病史,如起病年龄、生长发育情况,起病经过,用药史,家族史,个人生活习惯,既往有无全身性疾病。结合辅助检查,排除其他疾病,并经B超等检查明确诊断。 2...[详细]
宜根据患者的突出临床症状与体征、年龄及有否生育要求等而分别给予药物、手术或其他治疗。 1.肥胖与胰岛素抵抗 增加运动以减轻体重,纠正由肥胖而加剧的内分泌代谢紊乱,减轻胰岛素抵抗和高胰岛素血症,使IGF-1降低,IGfBP-1增加,同时SHBG增多使游离雄激素水平下降。减轻体重可使部分肥胖型PCOS者恢复排卵,并可预防2型糖尿病及心血管疾病的发生。二甲双胍1.5~2.5g/d,伴或不伴有糖尿病者均可使用,能有效地降低体重,改善胰岛素敏感性,降低胰岛素水平,使毛发减少甚至可恢复月经(25%)与排卵。由于肥胖和胰岛素抵抗是PCOS的主要病因,故凡可减轻体重与增加胰岛素敏感性的药物均可治疗本综合征。近年来,已有很多有关胰岛素增敏剂(insulin sensitizing agents)的治疗报道。噻唑烷酮(Thiazolidone)为一类口服胰岛素增敏剂,主要用于治疗糖尿病,如曲格列酮(Troglitazone)可明显减轻PCOS病人的高胰岛素血症和高雄激素血症,并有助于诱导排卵。Ciotta等报道,胰岛素增敏剂可明显降低血LH、雄激素水平、抑制胰岛素分泌,升高SHBG浓度,并可长期治疗,胰岛素增敏剂可能更适用于高胰岛素血症的PCOS患者。 2.药物诱导排卵 (1)氯米芬:是PCOS的首选药物,排卵率为60%~80%,妊娠率30%~50%。氯米芬与下丘脑-垂体水平的内源性雌激素竞争受体,抑制雌激素负反馈,增加GnRH分泌的脉冲频率,从而调整LH与FSH的分泌比率。氯米芬也直接促使卵巢合成和分泌雌激素。于自然月经周期或撤药性子宫出血的第5天开始,每天口服50mg,连续5次为1疗程,常于服药的3~10天(平均7天)排卵,多数在3~4个疗程内妊娠。若经3个治疗周期仍无排卵者,可将剂量递增至每天100~150mg,体重较轻者可考虑减少起始用量(25mg/d)。服用本药后,卵巢因过度刺激而增大(13.6%),血管舒张而有阵热感(10.4%)、腹部不适(5.5%)、视力模糊(1.5%)或有皮疹和轻度脱发等副作用。 治疗期间需记录月经周期的基础体温,监视排卵,或测定血清孕酮、雌二醇以证实有无排卵,指导下次疗程剂量的调整。若经氯米芬治疗6~12个月后仍无排卵或受孕者,可给予氯米芬加HCG或糖皮质激素、溴隐亭治疗或用HMG、FSH、GnRH等治疗。 (2)氯米芬与绒促性素(HCG)合用:停用氯米芬后第7天加用绒促性素(HCG) 2000~5000U肌注。 (3)糖皮质激素与氯米芬合用:肾上腺皮质激素的作用是基于它可抑制来自卵巢或肾上腺分泌的过多雄激素。通常选用地塞米松或泼尼松。泼尼松每天用量为7.5~10mg,2个月内有效率35.7%,闭经无排卵者的卵巢功能得到一定恢复。[收起]
宜根据患者的突出临床症状与体征、年龄及有否生育要求等而分别给予药物、手术或其他治疗。 1.肥胖与胰岛素抵抗 增加运动以减轻体重,纠正由肥胖而加剧的内分泌代谢紊乱,减轻胰岛素抵抗和高胰岛素血症,使IGF-1降低,IGfBP-1增加,同时SHBG增多使游离雄激素水平下降。减轻体重可使部分肥胖型PCOS者恢复排卵,并可预防2型糖尿病及心血管疾病的发生。二甲双胍1.5~2.5g/d,伴或不伴有糖尿病者均可使用,能有效地降低体重,改善胰岛素敏感性,降低胰岛素水平,使毛发减少甚至可恢复月经(25%)与排卵。由于肥胖和胰岛素抵抗是PCOS的主要病因,故凡可减轻体重与增加胰岛素敏感性的药物均可治疗本综合征。近...[详细]
多囊卵巢一旦出现则终身存在,只有症状和体征可改变或受到治疗的影响。
早期诊断、早期治疗、注意随访观察、积极防治并发的肿瘤及心血管疾病。


 2.雄激素过多 在PCOS中,几乎所有的雄激素生成均增多。而性激素结合球蛋白(SHBG)减少,游离雄激素增多,活性增强。至于过多的雄激素来源于卵巢或肾上腺众说不一。大剂量GnRH激动剂可降低促性腺激素,雄烯二酮和睾酮减少,而对来源于肾上腺的DHEAS无影响。据报道大约70%的PCOS患者为卵巢源性雄激素所致:①由于类固醇激素所需酶系功能紊乱,如芳香化酶缺乏,3β-醇甾脱氢酶不足或活性下降,P45OC17A调节异常,雌激素合成障碍,大量雄激素在外周(脂肪、肝、肾内)转换为雌酮。也有人认为卵巢发育不充分使芳香化酶的活性下降。②LH脉冲频率及振幅升高,刺激卵泡膜细胞及间质细胞增生和雄激素的生成。过多的雄激素促使卵泡闭锁,卵巢粒层细胞早期黄素化,生长停止,不能排卵,形成PCOS。 本病多发生在青春期月经初潮后,推测可能起因于性成熟前期,肾上腺功能失调,持续分泌过多雄激素。此外,在应用地塞米松前后测定卵巢和肾上腺静脉血中的各种雄激素水平,其结果支持卵巢和肾上腺是PCOS过多雄激素的共同来源,发现50%PCOS患者有肾上腺源性雄激素增多。 3.雌酮过多 PCOS妇女用孕酮等药物有撤退性子宫出血,服氯底酚胺可导致卵泡成熟排卵,月经来潮,这提示PCOS患者不但雄激素水平高,而且雌激素也增多。体内活性雌激素包括雌二醇(E2)和雌酮(E1),E2主要来源于卵巢,E1则来自卵巢、肾上腺及周围组织的转换。PCOS患者非周期性E1明显增多,E1/F2比率增高(正常E1/F2≤1),特别是肥胖者的脂肪多,芳香化酶活性高,外周组织转换增多,E1水平可更高,而且来源于外周组织的E1不受垂体促性腺激素的调节,无周期性变化。持续高水平的雌激素对下丘脑-垂体的反馈调节是不正常的。 4.细胞色素P450C17A调节失常 PCOS主要缺陷是下丘脑-垂体接受异常的反馈信号。这可能与卵巢和肾上腺本身的自分泌、旁分泌调节机制障碍有关。PCOS患者常伴17-羟孕酮(17-OHP)升高,这是由于卵泡膜细胞内或肾上腺网状带内P450C17A的调节机制失常所致。P450C17A具有17-羟化酶和17,20-链裂酶的双重活性,在?4将孕酮转换为17-OHP和雄烯二酮,在?5将孕烯醇酮衍变为17-羟孕烯醇酮和DHEA。 17-羟孕酮既是肾上腺合成皮质醇的重要前体物质.也是卵巢合成性激素特别是雄激素的重要前体。若给予PCOS患者GnRH-A或HCG(特别在用地塞米松抑制后),17-羟孕酮、雄烯二酮明显升高;而ACTH兴奋试验又能促使肾上腺的DHEA与17-OHP同时增多,提示卵巢和肾上腺网状带的P450C17A活性增高。因此,P450C17A活性调节异常是肾上腺和卵巢雄激素过量分泌的重要原因。但为什么会出现类固酮合成的调节异常尚不清楚。胰岛素/IGFs系统可刺激卵巢和肾上腺P450C17A mRNA表达及其活性。此外,CYP11A的侧链裂解酶基因编码区与产生过多雄激素有关。 5.胰岛素抵抗与高胰岛素血症 PCOS患者不论有无肥胖,多有不同程度的胰岛素抵抗与高胰岛素血症。近期发现大约有半数PCOS患者的发病与胰岛素受体丝氨酸磷酸化缺陷有关。因而认为胰岛素在其发病中占有重要地位。胰岛素与IGF-1通过IGF-1受体作用于卵泡膜细胞,促使雄烯二酮和睾酮合成。近年的研究发现,垂体邻近部位有胰岛素受体,或者同时存在的高IGF-1血症可促进LH刺激的卵泡膜细胞增生,导致雄激素过多和卵泡过早闭锁(图2)。Hasegawa用胰岛素增敏剂Troglitazone治疗PCOS,可使胰岛素水平降低,LH和雄激素水平相应降低也支持这一观点。胰岛素升高对调节SHBG的代谢有重要作用,可使肝脏SHBG生成减少,游离睾酮升高。此外,胰岛素受体丝氨酸磷酸化可抑制胰岛素受体活性,促进P450C17A的17,20-链裂酶活性。近年对位于染色体11pl5.5的胰岛素基因的5'-端可变数串联重复顺序(VNTR)的研究发现,胰岛素基因的VNTR是PCOS的一个主要易感位点(特别是排卵性PCOS)。说明胰岛素VNTR多态性是PCOS的遗传学因素。
2.雄激素过多 在PCOS中,几乎所有的雄激素生成均增多。而性激素结合球蛋白(SHBG)减少,游离雄激素增多,活性增强。至于过多的雄激素来源于卵巢或肾上腺众说不一。大剂量GnRH激动剂可降低促性腺激素,雄烯二酮和睾酮减少,而对来源于肾上腺的DHEAS无影响。据报道大约70%的PCOS患者为卵巢源性雄激素所致:①由于类固醇激素所需酶系功能紊乱,如芳香化酶缺乏,3β-醇甾脱氢酶不足或活性下降,P45OC17A调节异常,雌激素合成障碍,大量雄激素在外周(脂肪、肝、肾内)转换为雌酮。也有人认为卵巢发育不充分使芳香化酶的活性下降。②LH脉冲频率及振幅升高,刺激卵泡膜细胞及间质细胞增生和雄激素的生成。过多的雄激素促使卵泡闭锁,卵巢粒层细胞早期黄素化,生长停止,不能排卵,形成PCOS。 本病多发生在青春期月经初潮后,推测可能起因于性成熟前期,肾上腺功能失调,持续分泌过多雄激素。此外,在应用地塞米松前后测定卵巢和肾上腺静脉血中的各种雄激素水平,其结果支持卵巢和肾上腺是PCOS过多雄激素的共同来源,发现50%PCOS患者有肾上腺源性雄激素增多。 3.雌酮过多 PCOS妇女用孕酮等药物有撤退性子宫出血,服氯底酚胺可导致卵泡成熟排卵,月经来潮,这提示PCOS患者不但雄激素水平高,而且雌激素也增多。体内活性雌激素包括雌二醇(E2)和雌酮(E1),E2主要来源于卵巢,E1则来自卵巢、肾上腺及周围组织的转换。PCOS患者非周期性E1明显增多,E1/F2比率增高(正常E1/F2≤1),特别是肥胖者的脂肪多,芳香化酶活性高,外周组织转换增多,E1水平可更高,而且来源于外周组织的E1不受垂体促性腺激素的调节,无周期性变化。持续高水平的雌激素对下丘脑-垂体的反馈调节是不正常的。 4.细胞色素P450C17A调节失常 PCOS主要缺陷是下丘脑-垂体接受异常的反馈信号。这可能与卵巢和肾上腺本身的自分泌、旁分泌调节机制障碍有关。PCOS患者常伴17-羟孕酮(17-OHP)升高,这是由于卵泡膜细胞内或肾上腺网状带内P450C17A的调节机制失常所致。P450C17A具有17-羟化酶和17,20-链裂酶的双重活性,在?4将孕酮转换为17-OHP和雄烯二酮,在?5将孕烯醇酮衍变为17-羟孕烯醇酮和DHEA。 17-羟孕酮既是肾上腺合成皮质醇的重要前体物质.也是卵巢合成性激素特别是雄激素的重要前体。若给予PCOS患者GnRH-A或HCG(特别在用地塞米松抑制后),17-羟孕酮、雄烯二酮明显升高;而ACTH兴奋试验又能促使肾上腺的DHEA与17-OHP同时增多,提示卵巢和肾上腺网状带的P450C17A活性增高。因此,P450C17A活性调节异常是肾上腺和卵巢雄激素过量分泌的重要原因。但为什么会出现类固酮合成的调节异常尚不清楚。胰岛素/IGFs系统可刺激卵巢和肾上腺P450C17A mRNA表达及其活性。此外,CYP11A的侧链裂解酶基因编码区与产生过多雄激素有关。 5.胰岛素抵抗与高胰岛素血症 PCOS患者不论有无肥胖,多有不同程度的胰岛素抵抗与高胰岛素血症。近期发现大约有半数PCOS患者的发病与胰岛素受体丝氨酸磷酸化缺陷有关。因而认为胰岛素在其发病中占有重要地位。胰岛素与IGF-1通过IGF-1受体作用于卵泡膜细胞,促使雄烯二酮和睾酮合成。近年的研究发现,垂体邻近部位有胰岛素受体,或者同时存在的高IGF-1血症可促进LH刺激的卵泡膜细胞增生,导致雄激素过多和卵泡过早闭锁(图2)。Hasegawa用胰岛素增敏剂Troglitazone治疗PCOS,可使胰岛素水平降低,LH和雄激素水平相应降低也支持这一观点。胰岛素升高对调节SHBG的代谢有重要作用,可使肝脏SHBG生成减少,游离睾酮升高。此外,胰岛素受体丝氨酸磷酸化可抑制胰岛素受体活性,促进P450C17A的17,20-链裂酶活性。近年对位于染色体11pl5.5的胰岛素基因的5'-端可变数串联重复顺序(VNTR)的研究发现,胰岛素基因的VNTR是PCOS的一个主要易感位点(特别是排卵性PCOS)。说明胰岛素VNTR多态性是PCOS的遗传学因素。  6.肥胖 PCOS伴肥胖者(BMI≥25)占20%~60%。体脂分布不均匀。现知脂肪组织是类固醇激素的重要代谢场所,脂肪组织中的芳香化酶将外周雄激素转换为E1和E2。研究证实,雄烯二酮转换为E1的量与脂肪组织总量相关,高雄激素血症时SHBG下降,游离E2增加。雌激素使脂肪细胞生长、增殖。不同的内分泌环境能造成不同的肥胖体态,雄激素升高表现为上身肥胖(即男性型肥胖),而雌激素增多者为下身肥胖(即女性型肥胖)。体重增加常伴血胰岛素升高和SHBG及IGFBP下降,从而使游离性激素和IGF-1增多。这类患者常伴有糖耐量异常或2型糖尿病。 近来,Rouru等提出肥胖-瘦素-NPY轴可能是部分PCOS患者下丘脑-垂体-LH过度分泌的病因,即肥胖妇女的瘦素分泌增多,后者抑制下丘脑NPYmRNA表达和NPY的分泌,解除NPY对LH的抑制,促使LH大量释放。 7.高泌乳素血症 高泌乳素血症与PCOS的关系尚待进一步研究。
6.肥胖 PCOS伴肥胖者(BMI≥25)占20%~60%。体脂分布不均匀。现知脂肪组织是类固醇激素的重要代谢场所,脂肪组织中的芳香化酶将外周雄激素转换为E1和E2。研究证实,雄烯二酮转换为E1的量与脂肪组织总量相关,高雄激素血症时SHBG下降,游离E2增加。雌激素使脂肪细胞生长、增殖。不同的内分泌环境能造成不同的肥胖体态,雄激素升高表现为上身肥胖(即男性型肥胖),而雌激素增多者为下身肥胖(即女性型肥胖)。体重增加常伴血胰岛素升高和SHBG及IGFBP下降,从而使游离性激素和IGF-1增多。这类患者常伴有糖耐量异常或2型糖尿病。 近来,Rouru等提出肥胖-瘦素-NPY轴可能是部分PCOS患者下丘脑-垂体-LH过度分泌的病因,即肥胖妇女的瘦素分泌增多,后者抑制下丘脑NPYmRNA表达和NPY的分泌,解除NPY对LH的抑制,促使LH大量释放。 7.高泌乳素血症 高泌乳素血症与PCOS的关系尚待进一步研究。
 浙公网安备
33010902000463号
浙公网安备
33010902000463号



