-
科室:
妇科
-
别名:
postmenopausal endometrium
-
症状:
下腹痛
-
发病部位:
暂无
-
多发人群:
50岁以上女性多见
-
相关疾病:
暂无
子宫内膜癌又称子宫体癌,是指原发于子宫内膜的恶性肿瘤,其绝大多数是腺癌。绝经后妇女卵巢功能衰退,最终衰竭;由于雌激素水平逐渐降低,免疫功能发生衰减,致子宫内膜癌的发病率上升。
确切病因仍不清楚,可能与下列因素有关: 1.子宫内膜持续受雌激素刺激 与无排卵性功血、多囊卵巢综合征、功能性卵巢肿瘤、绝经后长期单一服用雌激素等,体内无孕酮对抗或孕酮不足,子宫内膜缺少周期性变化,而长期处于增生状态有关。 2.与子宫内膜增生过长有关 子宫内膜单纯型增生过长,约有1%发展为子宫内膜癌;复杂型增生过长约有3%;而不典型增生过长约有29%发展为子宫内膜癌。 3.体质因素 内膜癌易发生在肥胖、高血压、糖尿病者中,一般将肥胖-高血压-糖尿病称为子宫内膜癌三联症。未婚及不育也是内膜癌的高危因素。 4.绝经延迟 据有关报道,绝经年龄>52岁者子宫内膜癌的危险性是绝经年龄<45岁者的1.5~2.5倍。 5.遗传因素 有卵巢癌、肠癌或乳腺癌等家族史者,患内膜癌的可能性较无家族史者高。[收起]
确切病因仍不清楚,可能与下列因素有关: 1.子宫内膜持续受雌激素刺激 与无排卵性功血、多囊卵巢综合征、功能性卵巢肿瘤、绝经后长期单一服用雌激素等,体内无孕酮对抗或孕酮不足,子宫内膜缺少周期性变化,而长期处于增生状态有关。 2.与子宫内膜增生过长有关 子宫内膜单纯型增生过长,约有1%发展为子宫内膜癌;复杂型增生过长约有3%;而不典型增生过长约有29%发展为子宫内膜癌。 3.体质因素 内膜癌易发生在肥胖、高血压、糖尿病者中,一般将肥胖-高血压-糖尿病称为子宫内膜癌三联症。未婚及不育也是内膜癌的高危因素。 4.绝经延迟 据有关报道,绝经年龄>5...[详细]
子宫内膜癌的发生与宫颈癌相同,亦遵循由良性增生至癌变的演变过程。子宫内膜癌的发展过程是:正常增生的子宫内膜→囊性增生→腺瘤样增生→不典型增生和原位癌→浸润癌。单纯性子宫内膜增生为最轻度的内膜增生改变;囊性增生是癌发展中的早期阶段,仅有1.5%可发展为癌;子宫内膜上皮内瘤样病变(EIN)包括子宫腺瘤型增生过长伴细胞不典型增生及子宫内膜原位癌,亦称内膜癌的癌前病变。子宫内膜上皮内瘤样病变可自行逆转为正常内膜,也可发展为癌。由于内膜癌发展较慢,故有20%~40的内膜癌患者在确诊时病灶仍局限于内膜。 1.大体形态 肉眼观察子宫内膜癌可分2种类型: (1)弥漫型:子宫内膜大部或全部被癌组织侵犯,癌灶常呈菜花状从内膜表层长出并突向宫腔内,充满宫腔甚至脱出宫外。癌组织灰白或淡黄色,表面有出血、坏死,有时形成溃疡,当癌组织阻塞宫颈管时可致宫腔积脓。 (2)局限型:癌灶局限于宫腔,多见于宫底部或宫角部,呈息肉或小菜花状,表面有溃疡,易出血。局限型癌灶易侵犯肌层,有时病变虽小,但却已浸润深肌层。 2.组织学形态 子宫内膜癌有多种组织类型。根据癌组织结构表现及核的异型性程度,病理学可分3级,Ⅰ级(高分化);Ⅱ级(中度分化);Ⅲ级(低分化)。 (1)子宫内膜样腺癌:占80%~90%,内膜腺体高度异常增生,上皮复层,并形成筛孔状结构。癌细胞异型明显,核大、不规则、深染,核分裂活跃,分化差的腺癌腺体少,腺结构消失呈实性区域。 (2)腺癌伴鳞状上皮分化:腺癌组织中含有鳞状上皮成分。若腺癌中含有良性的鳞状上皮,称为棘腺癌。若腺癌中含有恶性鳞状上皮,称为鳞腺癌。 (3)透明细胞癌:癌细胞呈实性片状、腺管状或乳头状排列,癌细胞胞质丰富、透明,核异型居中,或由鞋钉状细胞组成。恶性程度高,易早期转移。 (4)浆液性腺癌:复杂的乳头样结构,裂隙样腺体,核异型性较大。恶性程度很高,易广泛累及肌层、脉管,或发生腹膜播散。 (5)未分化癌:很少见。癌细胞既无腺体分化,又无鳞状上皮分化倾向。 3.转移途径 多数子宫内膜癌生长缓慢,局限于内膜或子宫腔内时间较长。部分特殊病理类型的内膜癌,如浆液性乳头状腺癌、鳞腺癌、透明细胞癌和低分化癌可发展很快,短期内出现转移。转移途径主要为直接蔓延、淋巴转移,晚期可有血行转移。 (1)直接蔓延:病灶沿子宫内膜蔓延生长,向上可经宫角延至输卵管;向下可累及宫颈管,并继续蔓延至阴道。若癌组织向肌壁浸润可至子宫浆膜层,延至输卵管卵巢,并可广泛种植于盆腔腹膜、子宫直肠陷窝及大网膜。 (2)淋巴转移:为内膜癌的主要转移途径。当癌肿浸润至深肌层或扩散到宫颈管,或癌组织分化不良时,易发生淋巴转移。其转移途径与癌灶生长部位有关。宫底部癌灶沿阔韧带上部淋巴管网,经骨盆漏斗韧带至卵巢,向上至腹主动脉旁淋巴结;宫角部癌灶沿圆韧带至腹股沟淋巴结;子宫下段及宫颈管癌灶与宫颈癌淋巴转移途径相同,可至宫旁髂内、髂外、髂总淋巴结;子宫后壁癌灶可沿宫骶韧带至直肠淋巴结;前壁癌灶可扩散至膀胱淋巴结。内膜癌也可经淋巴管逆行引流至阴道前壁。 (3)血行转移:晚期可经血行转移至全身各器官,常见部位为肺、肝、骨。[收起]
子宫内膜癌的发生与宫颈癌相同,亦遵循由良性增生至癌变的演变过程。子宫内膜癌的发展过程是:正常增生的子宫内膜→囊性增生→腺瘤样增生→不典型增生和原位癌→浸润癌。单纯性子宫内膜增生为最轻度的内膜增生改变;囊性增生是癌发展中的早期阶段,仅有1.5%可发展为癌;子宫内膜上皮内瘤样病变(EIN)包括子宫腺瘤型增生过长伴细胞不典型增生及子宫内膜原位癌,亦称内膜癌的癌前病变。子宫内膜上皮内瘤样病变可自行逆转为正常内膜,也可发展为癌。由于内膜癌发展较慢,故有20%~40的内膜癌患者在确诊时病灶仍局限于内膜。 1.大体形态 肉眼观察子宫内膜癌可分2种类型: (1)弥漫型:子宫内膜大部或...[详细]
1.异常的子宫出血 是子宫内膜癌最常见的症状,其发生率占88%~96%,绝经后出血表现为血性分泌物或不规则阴道流血,量不多,大出血少见。绝经前期常误诊为功能失调性子宫出血,表现为经期延长,经量增多或间期出血。 2.阴道排液 多为瘤体渗出或继发感染的结果,可为血性液体、浆液性分泌物或脓性分泌物,伴有恶臭。颈管堵塞时,可以引起宫腔积脓,阴道异常分泌物增多常与子宫出血同时出现。 3.疼痛 多为晚期癌肿浸润周围组织或压迫神经而引起下腹痛、腰痛、并可放射至腿部。当宫腔积脓时,也可出现下腹痉挛性疼痛。 4.其他 晚期患者常出现贫血、消瘦、恶病质。 5.临床分期 采用国际妇产联盟1971年制定的临床分期(表1),对手术治疗者采用1988年制定的手术-病理分期(表2)。
 [收起]
1.异常的子宫出血 是子宫内膜癌最常见的症状,其发生率占88%~96%,绝经后出血表现为血性分泌物或不规则阴道流血,量不多,大出血少见。绝经前期常误诊为功能失调性子宫出血,表现为经期延长,经量增多或间期出血。 2.阴道排液 多为瘤体渗出或继发感染的结果,可为血性液体、浆液性分泌物或脓性分泌物,伴有恶臭。颈管堵塞时,可以引起宫腔积脓,阴道异常分泌物增多常与子宫出血同时出现。 3.疼痛 多为晚期癌肿浸润周围组织或压迫神经而引起下腹痛、腰痛、并可放射至腿部。当宫腔积脓时,也可出现下腹痉挛性疼痛。 4.其他 晚期患者常出现贫血、消瘦、恶病质。 5.临床分...[详细]
[收起]
1.异常的子宫出血 是子宫内膜癌最常见的症状,其发生率占88%~96%,绝经后出血表现为血性分泌物或不规则阴道流血,量不多,大出血少见。绝经前期常误诊为功能失调性子宫出血,表现为经期延长,经量增多或间期出血。 2.阴道排液 多为瘤体渗出或继发感染的结果,可为血性液体、浆液性分泌物或脓性分泌物,伴有恶臭。颈管堵塞时,可以引起宫腔积脓,阴道异常分泌物增多常与子宫出血同时出现。 3.疼痛 多为晚期癌肿浸润周围组织或压迫神经而引起下腹痛、腰痛、并可放射至腿部。当宫腔积脓时,也可出现下腹痉挛性疼痛。 4.其他 晚期患者常出现贫血、消瘦、恶病质。 5.临床分...[详细]
可合并全身症状 腹腔转移时可有腹部包块、腹胀、腹水,晚期可引起贫血、消瘦、恶病质及全身衰竭。
1.细胞学检查 有的作者报道,对患者进行宫颈管及阴道后穹窿涂片检查约60%为阳性,若在绝经期或绝经后妇女宫颈或阴道涂片中发现良性子宫内膜细胞,则预示2%~6%的潜隐性内膜癌,因此应提高警惕,进一步检查。但子宫内膜细胞平时不易脱落,一旦脱落又往往呈退行性变化,辨认困难,因此只能起到辅助诊断的作用。宫腔洗出液及吸出液的涂片检查可提高阳性率。经验丰富的细胞学家检查内膜细胞的阳性率可达90%~95%,但阴性不能除外内膜癌,且无法进行细胞分级,最后还需要分段诊刮。 子宫内膜癌合并腹水者,Ⅰ期无肌层浸润的有时也会在腹水中发现癌细胞。Marris报道3例内膜癌合并腹水,年龄为70多岁,无阴道出血,术前诊断为卵巢癌,内膜癌未侵入肌层,向宫腔凸出。此3例患者均为年老病人,其输卵管极度萎缩,更利于逆流。Creasman也提及有8%无肌层浸润之患者盆腔洗出液细胞阳性。 2.子宫内膜检查 分段刮宫,这是诊断子宫内膜癌所必要的检查。为了弄清病变是否累及颈管,刮宫时应分别从颈管和宫腔获得组织。颈管深度应根据子宫大小及颈管长度进行估计,先刮颈管,再测宫腔深度,以便判定临床期别,然后进行宫体及宫底部的刮宫,尤其注意刮取子宫双角的内膜,要小心全面地分段刮宫,刮出的内膜组织如为松脆的灰白色豆渣样组织,则应考虑为癌组织,此时应停止再刮,以免子宫穿孔而造成瘤细胞、血液及细菌污染腹腔。最后将刮出的组织分别送病理检查。内膜组织学检查为诊断的最后依据,其阳性率为90%。 内膜活检:可用于门诊病人检查,用Novak刮匙分别于宫腔四壁刮取内膜,阳性率为80%~90%,但阴性不能除外内膜癌,因有时所获得的组织太少,不能满足诊断要求,仍需分段刮宫。 3.肿瘤标志检查 (1)CAl9-9:存在于多种消化道腺癌中,苗勒管衍生的子宫及输卵管也合成CA19-9抗原。Scharl等报道,子宫内膜腺癌CAl9-9 57/70阳性,正常子宫内膜仅3/26阳性,故可成为子宫内膜癌的标志物。 (2)测定癌细胞的DNA含量:New-bury的研究结果表明,DNA倍体与子宫内膜癌的组织分级有关,组织分级越高,DNA倍率越高。据Izumis报道,检测子宫内膜癌68例,50%为非整倍体,细胞分化差的非整倍体占77.8%,高度分化的非整倍体只占33.5%,DNA指数与肿瘤分化程度呈负相关的关系。 Ieda M的研究表明,DNA倍体与肌层浸润及分期有关,深肌层浸润及Ⅲ、Ⅳ期的DNA异倍体率分别高于无肌层浸润及Ⅰ期者,DNA异倍体患者的生存率较二倍体者明显为低,5年生存率分别为65.9%及87.6%。提示DNA倍体为一重要的影响预后的因素。 (3)子宫内膜癌细胞周期时相中SPF的变化:SPF是反映细胞增殖活性的重要指标。SPF与肌层浸润及分期有关,随肌层浸润深度的增加及分期的提高,SPF明显升高。Fribery等报道,SPF值越高,预后越差,死亡率越高。薛凤霞等报道,SPF<17%者的5年生存率为79.1%,而>17%者为50.4%。 (4)血清CA125值测定:Duk的资料对110例子宫内膜癌患者测定血清CA125的结果发现:①CA125存在于所有子宫内膜癌组织中,特别是腺癌内;②子宫内膜癌CA125升高的占25%,其发生率随临床期别递增,Ⅰ期为13%,Ⅳ期为86%,Ⅰ、Ⅱ期有血管浸润及宫体外扩展者升高,第Ⅰ、Ⅱ期发现CA125升高时,应注意重订临床期别;③CA125水平随疾病的临床过程而变化,肿瘤发展及复发之前CA125即升高,特别是腹腔内有肿瘤时;④Ⅰ、Ⅱ期患者在治疗前若CA125升高,最后几乎均死于内膜癌,因此,治疗前测定CA125对估计预后有价值。 (5)QVX1是一种高分子量黏液样糖蛋白,XU Fengji采用双因子放射免疫分析法,测定了不同期别的子宫内膜癌患者45例血清中的OVX1水平,同时测定患者血清中CA125水平。正常人血清中OVX1值为(2.23±2.48)U/ml,2U/ml以下为界值,结果是4个期别的患者血清中OVX1大于7.2U/ml。OVX1的阳性率均比相应期别的CA125阳性率明显高。并且,OVX1与早期子宫内膜癌的期别和组织分级有关。OVX1在IA、IB、IC患者血清中的阳性率依次升高。组织分级越差者,OVX1阳性率亦越高。OVX1在Ⅰ期子宫内膜癌中的阳性率为64%,其敏感度高于CA125,因为OVX1和CA125无交叉关系,故可联合应用OVX1和CA125对子宫内膜癌进行检测,所以作者认为,OVX1可作为早期子宫内膜癌的肿瘤标志物,并且可联合应用其他较敏感的标志物对子宫内膜癌高危人群进行普查。[收起]
1.细胞学检查 有的作者报道,对患者进行宫颈管及阴道后穹窿涂片检查约60%为阳性,若在绝经期或绝经后妇女宫颈或阴道涂片中发现良性子宫内膜细胞,则预示2%~6%的潜隐性内膜癌,因此应提高警惕,进一步检查。但子宫内膜细胞平时不易脱落,一旦脱落又往往呈退行性变化,辨认困难,因此只能起到辅助诊断的作用。宫腔洗出液及吸出液的涂片检查可提高阳性率。经验丰富的细胞学家检查内膜细胞的阳性率可达90%~95%,但阴性不能除外内膜癌,且无法进行细胞分级,最后还需要分段诊刮。 子宫内膜癌合并腹水者,Ⅰ期无肌层浸润的有时也会在腹水中发现癌细胞。Marris报道3例内膜癌合并腹水,年龄为70多岁,无阴道出血...[详细]
1.宫腔镜检查 通过宫腔镜能直视宫腔内病灶的形态,位置及范围,对病灶进行定位活检或定位刮取组织,对发现较小的内膜癌很有意义,因此,宫腔镜是早期诊断内膜癌的可靠方法。同时,宫腔镜还能观察宫颈管有无浸润病灶。 子宫内膜癌在宫腔镜下观察有如下形态:①息肉型,表面为灰白色的粗糙不平的息肉样突起组织,并有曲张血管;②结节型,表现为较大的粗糙突起,表面有盘曲的血管;③乳头型,明显的结节状突起呈树枝状、葡萄状或绒团状;④溃疡型,凹陷表面有化脓感染、污浊、质脆。 关于宫腔镜检查能否引起癌细胞迁移的问题,目前尚无定论。一般认为,镜检导致癌细胞迁移的问题与操作者的技术水平、操作时间、膨宫介质的种类和注入速度及宫腔内压力有关。如能用CO2作膨宫介质,流速较小(30~40ml/min),宫腔压力较低(6.67~8.0kPa),操作时间在5min以内,则发生癌细胞迁移的机会将更小。 宫腔镜检查应避开急性盆腔炎症期。此外如患有心、肺疾病或体质虚弱者,应考虑用其他较安全的辅助诊断法。 2.显微子宫镜检查宫颈管 Goldbery认为,分段刮宫为盲目性操作,宫颈长度不明,只能随便采取活检,因此诊断的准确性不高。而显微子宫镜检查则对确定宫颈管是否受累有很大的优越性:①可直视颈管情况,如血管模样、乳头结构及子宫壁结构;②不需要扩张宫颈及探宫腔;③对宫颈黏膜上皮损伤极小;④可准确测量颈管长度;⑤易于采取病灶标本;⑧可在门诊进行。 3.B型超声检查 近年来应用阴道探头进行检查,可用来观察子宫内膜的厚度、肌层浸润深度及宫颈受累程度,从而可协助临床分期。Granberg S等的研究提示,子宫内膜厚度≤5mm者属于良性绝经后内膜,>9mm者可能为子宫内膜癌。子宫内膜癌患者的内膜平均厚度为17.7mm。因此,利用阴道B超是诊断子宫内膜癌的一种简易方法,其特异性为96%,敏感性为100%。除了观察子宫内膜厚度外,还能观察肌层浸润深度。 Schoenfeld将阴道超声测得的子宫矢状面上的肿瘤的前后径与内膜总宽度的比值作为预测有无深部癌浸润的标准,其值>30%有深部癌浸润,与病理标本对比,准确率84%,敏感性100%,特异性80%。从而可得到较为准确的临床分期以便手术时做适当处理。 Kurjiak报道,采用经阴道血流多普勒测定血流信号的变化来鉴别子宫内膜的良恶性病变。对308例各种子宫疾患的患者进行监测发现子宫内膜癌的阻力系数(RI)为0.34±0.05,正常人或良性疾患者RI>0.5,准确率为92.3%,并提出内膜异常血流图RI<0.4,RI在0.4~0.5应属可疑患者。 4.淋巴造影 用于术前发现淋巴结转移。根据其淋巴引流和转移过程,癌细胞可以直接到达骶前和腹主动脉淋巴结,也可沿圆韧带转移至腹股沟淋巴结。若肿瘤已侵犯子宫颈管,则其转移途径和原发宫颈癌一样,向髂淋巴结扩散。淋巴造影对子宫内膜癌的诊断价值,据Musumeci等报道,300例复发者中,61例淋巴造影阳性达47.5%,而无复发迹象者阳性率仅7.7%,从中也可看出造影对预后的预测意义。 5.CT及磁共振(MRI) 主要用于观察宫腔、宫颈病变,特别是肌层浸润的深度以及淋巴转移等,但直径小于2cm的淋巴结难于确认。[收起]
1.宫腔镜检查 通过宫腔镜能直视宫腔内病灶的形态,位置及范围,对病灶进行定位活检或定位刮取组织,对发现较小的内膜癌很有意义,因此,宫腔镜是早期诊断内膜癌的可靠方法。同时,宫腔镜还能观察宫颈管有无浸润病灶。 子宫内膜癌在宫腔镜下观察有如下形态:①息肉型,表面为灰白色的粗糙不平的息肉样突起组织,并有曲张血管;②结节型,表现为较大的粗糙突起,表面有盘曲的血管;③乳头型,明显的结节状突起呈树枝状、葡萄状或绒团状;④溃疡型,凹陷表面有化脓感染、污浊、质脆。 关于宫腔镜检查能否引起癌细胞迁移的问题,目前尚无定论。一般认为,镜检导致癌细胞迁移的问题与操作者的技术水平、操作时间、膨宫介质...[详细]
高育龄妇女出现不规则阴道出血,尤其绝经后阴道出血,结合上述临床特点及实验室、辅助检查即可诊断,确诊需要依靠病理检查。
根据子宫大小,肌层是否被癌浸润,宫颈管是否累及,癌细胞分化程度及病人全身情况,制定治疗方案。主要方法为手术、放疗、激素治疗和化疗,可单用或综合应用。 1.手术治疗 为首选的方案,尤其对早期病例。 (1)Ⅰ期:行筋膜外全子宫切除及双侧附件切除术。具有以下情况之一者应行选择性盆腔淋巴结及腹主动脉旁淋巴结切除和(或)清扫术: ①病理类型为透明细胞癌、浆液性癌、鳞形细胞癌、未分化癌、G2、G3子宫内膜样腺癌。 ②肌层浸润深度≥1/2。 ③癌累及宫腔50%以上或血清CA125有显著升高。 (2)Ⅱ期:行广泛全子宫及双侧附件切除术,盆腔及腹主动脉旁淋巴结清扫术。 手术进入腹腔后应先收集腹水或腹腔冲洗液做细胞学检查。术中全面探查,切除子宫附件后应立即剖视子宫,了解癌灶范围,浸润肌层深度,并送冰冻检查,确定有无子宫外的病变存在。癌组织应常规行雌、孕激素受体检测,作为术后选用辅助治疗的依据。 2.放射治疗 (1)术前放疗:可缩小病灶,创造手术条件或消除隐匿的转移病灶。Ⅱ、Ⅲ期病人,细胞分化不良,可在术前加用腔内照射或体外照射。腔内放疗结束后,1~2周内手术,体外照射结束4周后进行手术。 (2)术后放疗:用于手术未能完全切除的病灶,或可疑转移癌区,术后加用放疗,可补充手术范围不足,减少术后复发。Ⅱ期病人腹水中找到癌细胞或深肌层已有癌浸润,淋巴结已有转移,术后均需加放疗,60Co或直线加速器外照射。 (3)单纯放疗:腺癌虽对放射线不敏感,但在老年或有严重合并症不能耐受手术者,以及Ⅲ、Ⅳ期病人不宜手术者,放疗仍有一定效果。 3.药物治疗 (1)孕激素治疗:多用于晚期或复发癌不能手术切除者。对分化好,雌激素和孕激素受体阳性的内膜癌效果较好。宜大剂量长期应用。醋酸甲地孕酮(甲地孕酮)160mg/d口服;己酸羟孕酮500mg,每周2次,肌注。孕激素作用于癌细胞与孕激素受体结合形成复合物进入癌细胞核,延缓DNA和RNA复制,抑制癌细胞生长。长期应用可有水钠潴留、水肿或药物性肝炎等副作用,停药后可恢复。 (2)抗雌激素制剂治疗:他莫昔芬(tamoxifen,TAM)为一种非甾体类抗雌激素制剂,并有微弱的雌激素作用,用于治疗内膜癌的适应证与孕激素治疗相同。他莫昔芬(TAM) 10~20mg,2次/d,口服。他莫昔芬(TAM)可提高孕激素受体水平,受体水平低者可先用他莫昔芬(TAM)使孕激素受体含量增加后再用孕激素治疗或两者同时应用,可望提高疗效。副作用为类似围绝经期综合征表现,如潮热、急躁等,少量阴道流血或闭经。 (3)化疗药物治疗:为晚期或复发癌综合治疗措施之一,亦用于术后复发高危因素者治疗,以期减少盆腔外复发。常用化疗药物有多柔比星(阿霉素,ADM)、顺铂(DDP)、环磷酰胺(CTX)、氟尿嘧啶(5-Fu)、丝裂霉素(MMC)、依托泊苷(VP-16)等。可单独应用,或几种药物联合应用,也可与孕激素合并应用。[收起]
根据子宫大小,肌层是否被癌浸润,宫颈管是否累及,癌细胞分化程度及病人全身情况,制定治疗方案。主要方法为手术、放疗、激素治疗和化疗,可单用或综合应用。 1.手术治疗 为首选的方案,尤其对早期病例。 (1)Ⅰ期:行筋膜外全子宫切除及双侧附件切除术。具有以下情况之一者应行选择性盆腔淋巴结及腹主动脉旁淋巴结切除和(或)清扫术: ①病理类型为透明细胞癌、浆液性癌、鳞形细胞癌、未分化癌、G2、G3子宫内膜样腺癌。 ②肌层浸润深度≥1/2。 ③癌累及宫腔50%以上或血清CA125有显著升高。 (2)Ⅱ期:行广泛全子宫及双侧附件切除术,...[详细]
1.一般治疗效果 子宫内膜癌由于其发展缓慢,治疗效果比较好,5年生存率一般为60%~75%。 2.复发问题 Aalders分析379例复发性子宫内膜癌,局部复发者50%,远处转移者28%,局部及远处转移同时存在者21%。自第1次治疗至确定复发之平均时间,局部复发为14个月,转移为19个月,治疗后1年内复发者34%,3年内为76%,5年以上复发的10%,经治疗后32%局部复发的、5%转移的及2%局部及远处转移同时存在的在3~19年仍存活而无癌。 局部复发的可以考虑手术切除,或手术加放疗或化疗,在29例治愈的病人中,24例采用放射治疗或放射治疗加手术,16例还用了孕激素药物治疗。肺转移用孕激素类药物治疗的平均存活时间较未用激素类药物者长,前者为9个月,后者为2个月。 3.影响预后的因素 与预后有关的因素很多,主要与临床期别、淋巴转移、子宫肌层侵犯深度、细胞分化、组织类型、病人年龄等因素有关。 (1)临床期别:愈早期预后愈好。张惜阴对561例的分析,Ⅰ、Ⅱ、Ⅲ、Ⅳ期的5年存活率分别为74%、68%、36%及0%;Tiiti-nen分析881例子宫内膜腺癌总的5年存活率为82.1%,其中Ⅰa期为89.2%,Ⅰb期为82.9%,Ⅱ期为72.8%,Ⅳ期为0%。 (2)淋巴转移:有淋巴转移者预后差,Berman的综合资料见表3。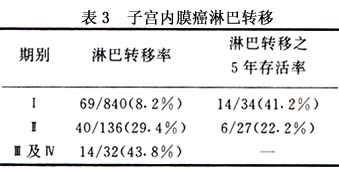 (3)子宫肌层浸润深度:Ⅰ期子宫内膜癌中,子宫肌层浸润深度与淋巴转移和预后有很密切的关系。浅表肌层浸润癌的淋巴转移率低,而深肌层浸润者转移率高,同时阴道穹窿复发及远处转移均增高。Co-hen报道,无肌层浸润及浅肌层浸润的5年存活率为80%~85%,深肌层浸润者为60%。协和医院的资料证明,无肌层浸润者5年存活率为88.2%,浅肌层浸润者为86.2%,深肌层浸润者为47.3%。 (4)细胞分化程度与预后的关系:极为密切,细胞低分化的癌,其肌层浸润深度、淋巴转移、宫颈转移、阴道转移及远处转移就高,预后也就差,分化低的肿瘤更有血循播散的可能。Tiitinen报道,Ⅰ期5年存活率按1,2,3级分别为80.7%,81%及50.5%,Ⅱ期1,2,3级分别为73.5%,59.1%和48.4%,显然3级的预后比1,2级差。 (5)组织类型:现今一致公认,腺棘癌与单纯腺癌预后较好,而腺癌、乳头状浆液性腺癌预后差。陈毅南报道149例内膜癌、腺癌和腺棘癌5年存活率分别为75%及84.6%,而腺鳞癌只有37.5%,透明细胞癌组织分化不良者居多,故预后不良,Ⅰ期患者5年存活率仅为42%。 (6)年龄:年龄越大,预后越差。据国外报道,小于60岁的病人5年存活率为90%,而60岁以上者仅65%,原因可能是:①老年人的肿瘤多为分化不良;②分化差的病例需要积极的治疗,而老年人常不易耐受。 (7)甾体激素受体:Ehrlich报道,用DCC法测定性激素受体,发现孕激素受体比雌激素受体更有用,如孕激素受体阴性,Ⅰ期患者的复发率明显高于孕激素受体阳性者,其比例为37.2%与7%,雌激素受体阴性者,其复发率为41.2%,阳性者12.7%。总的说,患者的生存率与孕激素受体含量有关,孕激素受体阳性者,其生存率明显高于阴性者。 (8)外源性雌激素与预后的关系:最近注意到,用过雌激素的子宫内膜癌病人的预后比未用过者好。Smith分析173例内膜癌,其中62例未用过雌激素,也无肥胖,糖尿病等,这类患者比用过雌激素的临床期别较晚,细胞分化较差,死亡率较高,5年内死亡的共13例,未用过雌激素的死亡10例,而用过雌激素只3例。 (9)其他因素:如脉管内有癌栓、腹腔细胞学阳性者预后均较差。[收起]
1.一般治疗效果 子宫内膜癌由于其发展缓慢,治疗效果比较好,5年生存率一般为60%~75%。 2.复发问题 Aalders分析379例复发性子宫内膜癌,局部复发者50%,远处转移者28%,局部及远处转移同时存在者21%。自第1次治疗至确定复发之平均时间,局部复发为14个月,转移为19个月,治疗后1年内复发者34%,3年内为76%,5年以上复发的10%,经治疗后32%局部复发的、5%转移的及2%局部及远处转移同时存在的在3~19年仍存活而无癌。 局部复发的可以考虑手术切除,或手术加放疗或化疗,在29例治愈的病人中,24例采用放射治疗或放射治疗加手术,16例还用了孕激素...[详细]
(3)子宫肌层浸润深度:Ⅰ期子宫内膜癌中,子宫肌层浸润深度与淋巴转移和预后有很密切的关系。浅表肌层浸润癌的淋巴转移率低,而深肌层浸润者转移率高,同时阴道穹窿复发及远处转移均增高。Co-hen报道,无肌层浸润及浅肌层浸润的5年存活率为80%~85%,深肌层浸润者为60%。协和医院的资料证明,无肌层浸润者5年存活率为88.2%,浅肌层浸润者为86.2%,深肌层浸润者为47.3%。 (4)细胞分化程度与预后的关系:极为密切,细胞低分化的癌,其肌层浸润深度、淋巴转移、宫颈转移、阴道转移及远处转移就高,预后也就差,分化低的肿瘤更有血循播散的可能。Tiitinen报道,Ⅰ期5年存活率按1,2,3级分别为80.7%,81%及50.5%,Ⅱ期1,2,3级分别为73.5%,59.1%和48.4%,显然3级的预后比1,2级差。 (5)组织类型:现今一致公认,腺棘癌与单纯腺癌预后较好,而腺癌、乳头状浆液性腺癌预后差。陈毅南报道149例内膜癌、腺癌和腺棘癌5年存活率分别为75%及84.6%,而腺鳞癌只有37.5%,透明细胞癌组织分化不良者居多,故预后不良,Ⅰ期患者5年存活率仅为42%。 (6)年龄:年龄越大,预后越差。据国外报道,小于60岁的病人5年存活率为90%,而60岁以上者仅65%,原因可能是:①老年人的肿瘤多为分化不良;②分化差的病例需要积极的治疗,而老年人常不易耐受。 (7)甾体激素受体:Ehrlich报道,用DCC法测定性激素受体,发现孕激素受体比雌激素受体更有用,如孕激素受体阴性,Ⅰ期患者的复发率明显高于孕激素受体阳性者,其比例为37.2%与7%,雌激素受体阴性者,其复发率为41.2%,阳性者12.7%。总的说,患者的生存率与孕激素受体含量有关,孕激素受体阳性者,其生存率明显高于阴性者。 (8)外源性雌激素与预后的关系:最近注意到,用过雌激素的子宫内膜癌病人的预后比未用过者好。Smith分析173例内膜癌,其中62例未用过雌激素,也无肥胖,糖尿病等,这类患者比用过雌激素的临床期别较晚,细胞分化较差,死亡率较高,5年内死亡的共13例,未用过雌激素的死亡10例,而用过雌激素只3例。 (9)其他因素:如脉管内有癌栓、腹腔细胞学阳性者预后均较差。[收起]
1.一般治疗效果 子宫内膜癌由于其发展缓慢,治疗效果比较好,5年生存率一般为60%~75%。 2.复发问题 Aalders分析379例复发性子宫内膜癌,局部复发者50%,远处转移者28%,局部及远处转移同时存在者21%。自第1次治疗至确定复发之平均时间,局部复发为14个月,转移为19个月,治疗后1年内复发者34%,3年内为76%,5年以上复发的10%,经治疗后32%局部复发的、5%转移的及2%局部及远处转移同时存在的在3~19年仍存活而无癌。 局部复发的可以考虑手术切除,或手术加放疗或化疗,在29例治愈的病人中,24例采用放射治疗或放射治疗加手术,16例还用了孕激素...[详细]
1.定期防癌检查。 2.对更年期月经紊乱和绝经后不规则阴道出血应及时诊断性刮宫,除外恶性肿瘤后再对症治疗。 3.对高危患者应注意及时检查。 4.正确指导使用激素替代疗法,服用雌激素同时,还应每月服用孕激素不少于10天,以保护子宫内膜,防止增生。使用HRT者应定期妇科检查。有家族史、乳腺增生或子宫内膜增生者慎用。 5.由于长期大剂量服用他莫昔芬(三苯氧胺)可引起子宫内膜增生,甚至能有子宫内膜癌发生的可能,因此对乳腺癌术后服用他莫昔芬(三苯氧胺)患者,应定期行妇科检查,并应作B超检查,了解子宫内膜厚度,如内膜>5mm,或有阴道不规则出血,则应及时行诊断性刮宫。[收起]
1.定期防癌检查。 2.对更年期月经紊乱和绝经后不规则阴道出血应及时诊断性刮宫,除外恶性肿瘤后再对症治疗。 3.对高危患者应注意及时检查。 4.正确指导使用激素替代疗法,服用雌激素同时,还应每月服用孕激素不少于10天,以保护子宫内膜,防止增生。使用HRT者应定期妇科检查。有家族史、乳腺增生或子宫内膜增生者慎用。 5.由于长期大剂量服用他莫昔芬(三苯氧胺)可引起子宫内膜增生,甚至能有子宫内膜癌发生的可能,因此对乳腺癌术后服用他莫昔芬(三苯氧胺)患者,应定期行妇科检查,并应作B超检查,了解子宫内膜厚度,如内膜>5mm,或有阴道不规则出血,则应及时行诊...[详细]



 (3)子宫肌层浸润深度:Ⅰ期子宫内膜癌中,子宫肌层浸润深度与淋巴转移和预后有很密切的关系。浅表肌层浸润癌的淋巴转移率低,而深肌层浸润者转移率高,同时阴道穹窿复发及远处转移均增高。Co-hen报道,无肌层浸润及浅肌层浸润的5年存活率为80%~85%,深肌层浸润者为60%。协和医院的资料证明,无肌层浸润者5年存活率为88.2%,浅肌层浸润者为86.2%,深肌层浸润者为47.3%。 (4)细胞分化程度与预后的关系:极为密切,细胞低分化的癌,其肌层浸润深度、淋巴转移、宫颈转移、阴道转移及远处转移就高,预后也就差,分化低的肿瘤更有血循播散的可能。Tiitinen报道,Ⅰ期5年存活率按1,2,3级分别为80.7%,81%及50.5%,Ⅱ期1,2,3级分别为73.5%,59.1%和48.4%,显然3级的预后比1,2级差。 (5)组织类型:现今一致公认,腺棘癌与单纯腺癌预后较好,而腺癌、乳头状浆液性腺癌预后差。陈毅南报道149例内膜癌、腺癌和腺棘癌5年存活率分别为75%及84.6%,而腺鳞癌只有37.5%,透明细胞癌组织分化不良者居多,故预后不良,Ⅰ期患者5年存活率仅为42%。 (6)年龄:年龄越大,预后越差。据国外报道,小于60岁的病人5年存活率为90%,而60岁以上者仅65%,原因可能是:①老年人的肿瘤多为分化不良;②分化差的病例需要积极的治疗,而老年人常不易耐受。 (7)甾体激素受体:Ehrlich报道,用DCC法测定性激素受体,发现孕激素受体比雌激素受体更有用,如孕激素受体阴性,Ⅰ期患者的复发率明显高于孕激素受体阳性者,其比例为37.2%与7%,雌激素受体阴性者,其复发率为41.2%,阳性者12.7%。总的说,患者的生存率与孕激素受体含量有关,孕激素受体阳性者,其生存率明显高于阴性者。 (8)外源性雌激素与预后的关系:最近注意到,用过雌激素的子宫内膜癌病人的预后比未用过者好。Smith分析173例内膜癌,其中62例未用过雌激素,也无肥胖,糖尿病等,这类患者比用过雌激素的临床期别较晚,细胞分化较差,死亡率较高,5年内死亡的共13例,未用过雌激素的死亡10例,而用过雌激素只3例。 (9)其他因素:如脉管内有癌栓、腹腔细胞学阳性者预后均较差。
(3)子宫肌层浸润深度:Ⅰ期子宫内膜癌中,子宫肌层浸润深度与淋巴转移和预后有很密切的关系。浅表肌层浸润癌的淋巴转移率低,而深肌层浸润者转移率高,同时阴道穹窿复发及远处转移均增高。Co-hen报道,无肌层浸润及浅肌层浸润的5年存活率为80%~85%,深肌层浸润者为60%。协和医院的资料证明,无肌层浸润者5年存活率为88.2%,浅肌层浸润者为86.2%,深肌层浸润者为47.3%。 (4)细胞分化程度与预后的关系:极为密切,细胞低分化的癌,其肌层浸润深度、淋巴转移、宫颈转移、阴道转移及远处转移就高,预后也就差,分化低的肿瘤更有血循播散的可能。Tiitinen报道,Ⅰ期5年存活率按1,2,3级分别为80.7%,81%及50.5%,Ⅱ期1,2,3级分别为73.5%,59.1%和48.4%,显然3级的预后比1,2级差。 (5)组织类型:现今一致公认,腺棘癌与单纯腺癌预后较好,而腺癌、乳头状浆液性腺癌预后差。陈毅南报道149例内膜癌、腺癌和腺棘癌5年存活率分别为75%及84.6%,而腺鳞癌只有37.5%,透明细胞癌组织分化不良者居多,故预后不良,Ⅰ期患者5年存活率仅为42%。 (6)年龄:年龄越大,预后越差。据国外报道,小于60岁的病人5年存活率为90%,而60岁以上者仅65%,原因可能是:①老年人的肿瘤多为分化不良;②分化差的病例需要积极的治疗,而老年人常不易耐受。 (7)甾体激素受体:Ehrlich报道,用DCC法测定性激素受体,发现孕激素受体比雌激素受体更有用,如孕激素受体阴性,Ⅰ期患者的复发率明显高于孕激素受体阳性者,其比例为37.2%与7%,雌激素受体阴性者,其复发率为41.2%,阳性者12.7%。总的说,患者的生存率与孕激素受体含量有关,孕激素受体阳性者,其生存率明显高于阴性者。 (8)外源性雌激素与预后的关系:最近注意到,用过雌激素的子宫内膜癌病人的预后比未用过者好。Smith分析173例内膜癌,其中62例未用过雌激素,也无肥胖,糖尿病等,这类患者比用过雌激素的临床期别较晚,细胞分化较差,死亡率较高,5年内死亡的共13例,未用过雌激素的死亡10例,而用过雌激素只3例。 (9)其他因素:如脉管内有癌栓、腹腔细胞学阳性者预后均较差。 浙公网安备
33010902000463号
浙公网安备
33010902000463号